
| 实验编号 | 实验目的 | 温度/ | pH | 浓度/(mg.L-1) | |
| ① | 为提供参照 | 25 | 3 | H2O2 | Fe2+ |
| ② | 探究温度对降解反应速率的影响 | 204 | 16.8 | ||
| ③ | 25 | 10 | 204 | 16.8 | |
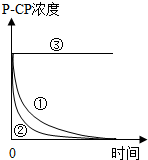
分析 (1)对比实验的基本思想是控制变量法,可以在温度相同时,变化浓度,或者在浓度相等时,变化温度;
(2)根据实验①②的数据来回答;
(3)根据实验数据内容进行分析;
(4)根据实验数据内容进行分析.
解答 解;(1)对比实验的基本思想是控制变量法,温度相同时,变化浓度,在浓度相等时,变化温度,故答案为:40;3;204;16.8;探究pH对降解反应速率的影响;
(2)根据实验数据内容可以看出温度升高,降解反应速率增加;由于过氧化氢在温度过高时易分解,所以温度过高时,降解反应较难发生,故答案为:加快;过氧化氢在温度过高时易分解;
(3)根据实验数据内容可以看出pH=10时,反应速率趋向于零,故答案为:反应速率趋向于零;
(4)根据实验数据内容可以看出,将所取样品迅速加入到一定量的NaOH溶液中,使pH为10,就可使样品中的降解反应立即停止下来,故答案为:将所取样品迅速加入到一定量的NaOH溶液中,使pH为10.
点评 本题考查学生化学平衡状态以及化学反应速率知识,要求学生具有分析和解决问题的能力,难度较大.


 巧学巧练系列答案
巧学巧练系列答案科目:初中化学 来源: 题型:选择题
| A. | PM2.5系可吸入颗粒物,其直径比分子小 | |
| B. | 空气质量级别值越大空气质量越好 | |
| C. | “水华”与“赤潮”诱发的根源不同 | |
| D. | 垃圾是放错位置的资源 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某品牌饮品为绿色食品,不含任何化学物质 | |
| B. | 科研人员发明了一种特殊催化剂,可以将水变为汽油 | |
| C. | 有关部分利用明矾对饮用水进行消毒杀菌,从而解决灾民饮水难的问题 | |
| D. | 回收处理废旧电池,既可节约资源又可减少环境污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 在初中化学中,我们学习了溶液的有关知识.右图是KNO3的溶解度曲线.
在初中化学中,我们学习了溶液的有关知识.右图是KNO3的溶解度曲线.
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铵态氮肥与碱共热放出有刺激性气味的气体 | |
| B. | 带火星的木条伸入到盛有氧气的集气瓶中,木条复燃 | |
| C. | 给水通直流电,产生气泡 | |
| D. | 敞口放置的浓盐酸瓶口产生白雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | A | B | C | D |
| 实验操作 | 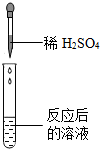 | 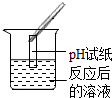 | 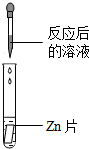 | 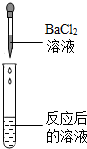 |
| 实验现象 | 无气泡产生 | 试纸变色,对照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 猜想二错误 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com