
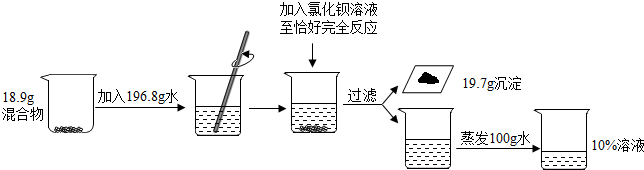
分析 (1)根据碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠进行分析;
(2)根据化学方程式中各物质的质量比分析解答;
(3)根据化学方程式,结合沉淀的质量来计算出碳酸钠的质量即可解答;
(4)随着反应的进行,碳酸钠的质量逐渐减少,氯化钠的质量逐渐增大;
(5)根据质量守恒定律计算所得溶液的质量;
(6)根据化学方程式,结合沉淀的质量来计算出消耗氯化钡的质量即可解答.
解答 解:(1)碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl;
(2)设碳酸钠的质量为x,消耗氯化钡的质量为y,生成氯化钠的质量为z,
Na2CO3+BaCl2=BaCO3↓+2NaCl
106 208 197 117
x y 19.7g z
$\frac{106}{x}$=$\frac{208}{y}$=$\frac{197}{19.7g}$=$\frac{117}{z}$
x=10.6g
y=20.8g
z=11.7g
(3)混合物中氯化钠和碳酸钠质量的最简整数比:(18.9g-10.6g):10.6g=83:106;
(4)在滴加氯化钡溶液的过程中,烧杯中溶质随着反应的进行,碳酸钠的质量逐渐减少,氯化钠的质量逐渐增大;
(5)所得溶液质量为:$\frac{11.7g+18.9g-10.6g}{10%}$+100g=300g;
(6)所用氯化钡溶液中溶质质量分数为:$\frac{20.8g}{300g+19.7g-18.9g-196.8g}$×100%=20%.
故答案为;(1)Na2CO3+BaCl2=BaCO3↓+2NaCl;
(2)$\frac{106}{x}$=$\frac{197}{19.7g}$;
(3)83:106;
(4)随着反应的进行,碳酸钠的质量逐渐减少,氯化钠的质量逐渐增大;
(5)300g;
(6)20%.
点评 本题考查了氯化钠与碳酸钠的化学性质,同时考查了化学方程式的书写以及根据化学方程式计算溶液的质量分数,要求学生熟练掌握常见物质的化学性质以及相关的化学方程式.


科目:初中化学 来源: 题型:选择题
| A. | 生活垃圾分类处理,禁止随意焚烧 | |
| B. | 化石燃料的大量使用是形成雾霾天气主要原因 | |
| C. | 为尽情欢度春节,大量燃放烟花爆竹 | |
| D. | 私家车剧增,也是导致PM2.5增加的重要原因 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用肥皂水鉴别软水和硬水 | |
| B. | 用带火星的木条鉴别空气和氧气 | |
| C. | 用稀HCl除去Na2SO4溶液中少量的Na2CO3 | |
| D. | 用溶解,过滤的方法除去MnO2粉末中少量的KCl固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 课外活动中,化学兴趣小组的同学们进行了以下实验.为了验证质量守恒定律,同学们设计了如图所示的实验装置,其中气球的作用是:缓冲作用;镁粉燃烧的现象是产生耀眼的白光,放热,生成白色粉末;请从微观的角度解释燃烧前后质量守恒的原因化学反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化.
课外活动中,化学兴趣小组的同学们进行了以下实验.为了验证质量守恒定律,同学们设计了如图所示的实验装置,其中气球的作用是:缓冲作用;镁粉燃烧的现象是产生耀眼的白光,放热,生成白色粉末;请从微观的角度解释燃烧前后质量守恒的原因化学反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
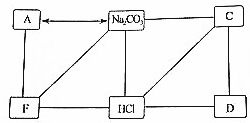 图是六种物质之间的转化关系.用“-”表示两种物质之间能发生反应,用“→”表示一种物质可以转化成另一种物质.A,B,C,D,E,F六种物质中,B,E已给出,其他四种物质分别为碱,盐,氧化物和黑色的金属粉末中的一种,回答下列问题:
图是六种物质之间的转化关系.用“-”表示两种物质之间能发生反应,用“→”表示一种物质可以转化成另一种物质.A,B,C,D,E,F六种物质中,B,E已给出,其他四种物质分别为碱,盐,氧化物和黑色的金属粉末中的一种,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
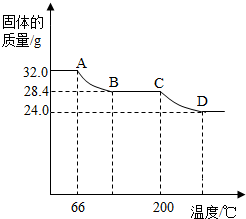
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Zn(NO3)2、AgNO3 | B. | Zn(NO3)2、Cu(NO3)2、AgNO3 | ||
| C. | Zn(NO3)2、Cu(NO3)2 | D. | Zn(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
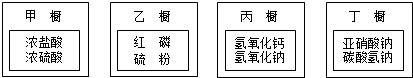
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com