
下图是某省生产的某种加钙食盐包装标签上的部分文字,请仔细阅读后回答问题:
(1)包装标签上的钙含量是指 (填“单质钙”“碳酸钙”或“钙元素”)。
(2)为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是 。
(3)为了测定此盐中的钙元素含量,取10 g这种盐溶于水,加入足量盐酸,生成0.011 mg二氧化碳。请计算此加钙食盐中钙元素的质量分数。
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:初中化学 来源: 题型:计算题
(5分)超市卖的纯碱产品中往往会含有少量的氯化钠,为了测定其组成,某校化学兴趣小组的同学对其进行了如下实验:
(1)用试管取适量样品,先向其中加入过量稀硝酸,再滴入适量硝酸银溶液,若观察到 ,则证明该样品中含有氯化钠。
(2)为测定该产品中碳酸钠的含量,进行如下定量实验: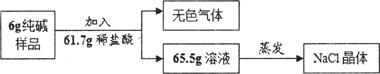
①根据质量守恒定律,该实验所得无色气体的质量是 。
②计算该6g纯碱样品中碳酸钠的质量,请写出计算过程。(计算结果精确至O.lg)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
葡萄糖是生命活动中不可缺少的物质,它在人体内能直接参与新陈代谢过程。
| | 部分性质 | 生理作用 |
| 葡萄糖 化学式: C6H12O6 | 白色结晶或颗粒状粉末,味甜;易溶于水;具有还原性,葡萄糖溶液与新制氢氧化铜悬浊液反应生成砖红色沉淀 | 葡萄糖为机体所需能量的主要来源,能促进肝脏的解毒功能,对肝脏有保护作用 |

 C6H12O7+Cu2O↓+2H2O
C6H12O7+Cu2O↓+2H2O 查看答案和解析>>
科目:初中化学 来源: 题型:计算题
“轻钙”是一种颗粒极细、纯度很高的碳酸钙粉末,有广泛的用途,如用来制作钙片、钙盐等。我市某轻钙厂用当地丰富的石灰石,通过如下流程制“轻钙”:
(1)碳酸钙中钙元素的质量分数是____%,食盐中添加碳酸钙有助于防止人体缺钙引起的_______________________(填 “骨骼疏松症”或“贫血病”)。
(2)石灰石经高温转化为A和B,该反应属于_____________(填基本反应类型)。
(3)沉淀池中得到的块状残渣可能含有未烧透的石灰石。技术人员用盐酸进行检验,观察到 ,证明残渣中含有石灰石。
(4)工厂技术人员提出,利用碳酸钠代替二氧化碳与氢氧化钙反应,在生成碳酸钙的同时还可得到氢氧化钠。请通过计算求:利用这种方法生产50t碳酸钙时,能得到氢氧化钠的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6 g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5 g时,烧杯内溶液的总质量为40.3 g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算: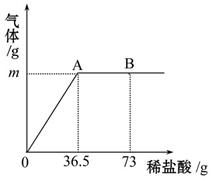
(1)A点产生气体的质量为__________;
(2)试样中碳酸钠的质量分数(结果精确到0.1%);
(3)B点时,烧杯内溶液中溶质的化学式为_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
相同质量的M、N两种活泼金属,分别与足量的稀盐酸在室温下发生反应(M、N在生成物中的化合价均为+2价),生成H2的质量m和反应时间t的关系如图所示。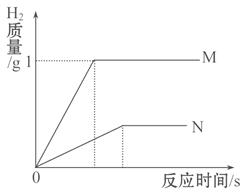
(1)金属活动性顺序是M比N________(填“强”或“弱”);相对原子质量是M比N的________(填“大”或“小”)。
(2)M与稀盐酸反应结束后,消耗稀盐酸中溶质的质量为________g。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
向碳酸钠和氯化钠的混合物15.6 g中加入100 g稀盐酸,恰好完全反应后,得到111.2 g溶液。试计算:
(1)产生二氧化碳多少克?
(2)所得溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
已知烧杯中装有200g硫酸和硫酸锌混合溶液,其中含硫酸锌12.1g.向烧杯中逐渐加入锌粒,放出气体质量与加入锌粒质量的关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.请计算:
(1)m=_________(2)原混合溶液中H2SO4的质量分数为_________.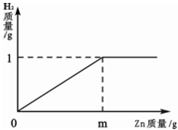
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com