
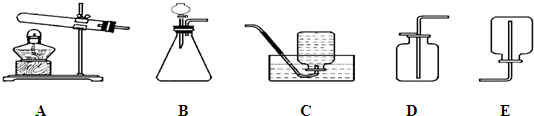
A、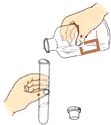 倾倒液体 |
B、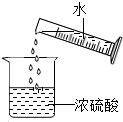 稀释浓硫酸 稀释浓硫酸 |
C、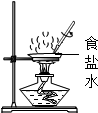 蒸发食盐水 |
D、 加热液体 |
| 1 |
| 3 |
| 1 |
| 3 |


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:
 根据图回答下列问题:
根据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
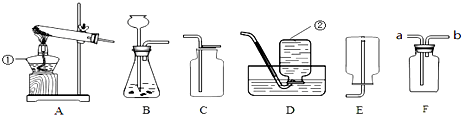
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验方案 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL 5%过氧化氢溶液的试管中 | 带火星木条不复燃 | 过氧化氢溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%过氧化氢溶液的试管中加入1g氧化铜固体,将一根带火星的木条伸入试管.观察现象.待反应结束后将试管里的剩余物进行过滤、洗涤、干燥、称量.对比反应前后氧化铜的质量 | 称得固体质量为1g. | 猜想Ⅰ成立.反应前后氧化铜的质量相等. |
| 实验三:向盛有5mL5%过氧化氢溶液的试管中加入1g | 没有气泡产生,带火星木条不复燃 | 猜想Ⅱ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com