【答案】
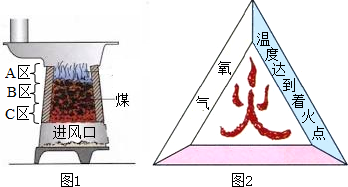
分析:(1)根据煤炉中各部分发生的反应及反应的特点分析;
(2)根据燃烧的条件和是演的过程分析;
(3)[实验探究1]II.①根据质量守恒定律确定煤中含有的元素;
②根据二氧化碳、二氧化硫的性质分析;
[实验探究2]根据二氧化硫、二氧化碳吗的性质分析;
[拓展延伸]①根据二氧化硫与水反应的性质分析;
②根据硫燃烧的反应进行计算.
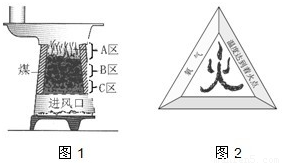
解答:解:(1)在煤炉上方即A区一氧化碳燃烧生成了二氧化碳,反应的方程式是:2CO+O
2 
2CO
2,在煤炉中间即B区在高温条件下二氧化碳和碳反应生成了一氧化碳,反应的方程式是:CO
2+C

2CO,该反应由两种物质生成了一种物质,属于化合反应;
(2)由燃烧的条件可知,图中缺少的一个条件是可燃物.由实验的过程可知,酒精能燃烧水不能燃烧,说明了燃烧需要可燃物;
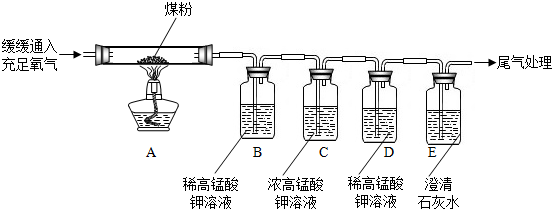
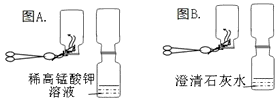
(3)[实验探究1]II.①图A中稀高锰酸钾溶液褪色,说明煤燃烧生成二氧化硫,说明煤中含硫元素,图B中澄清石灰水变浑浊,说明煤燃烧生成二氧化碳,说明煤中含碳元素;
②由于二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,不能根据能使澄清的石灰水变浑浊证明可燃物中含有硫元素.
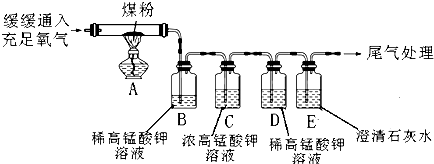
[实验探究2]①通过B装置中的稀高锰酸钾溶液褪色,说明煤燃烧生成二氧化硫,说明煤中含硫元素.所以B装置的作用是:证明煤中含有硫元素;
②C装置的作用是:除去气体中的二氧化硫,避免对后面实验的干扰;
③当观察到:装置D中稀高锰酸钾溶液不变色,E中澄清石灰水变浑浊,即能证明煤中含有碳元素;
[拓展延伸]①由于二氧化硫能与水化合生成亚硫酸,所以,SO
2遇雨水会形成酸雨;
②1000t原煤含硫:1000t×1%=10t
设:10t硫可以产生二氧化硫X
S+O
2
SO
232 64
10t X
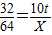
解得:X=20t
故答为:(1)2CO+O
2 
2CO
2,CO
2+C
2CO,化合;(2)可燃物,①;(3)[实验探究1]II①硫,碳;②二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊;①证明煤中含有硫元素;②除去气体中的二氧化硫,避免对后面实验的干扰;③不变色,变浑浊;(4)10t.
点评:本题考查了常见气体性质的探究,解答时可以依据物质的性质并结合题干叙述进行分析,该类题能很好的考查学生的思维能力,分析和解决问题的能力.

 2CO2,在煤炉中间即B区在高温条件下二氧化碳和碳反应生成了一氧化碳,反应的方程式是:CO2+C
2CO2,在煤炉中间即B区在高温条件下二氧化碳和碳反应生成了一氧化碳,反应的方程式是:CO2+C  2CO,该反应由两种物质生成了一种物质,属于化合反应;
2CO,该反应由两种物质生成了一种物质,属于化合反应; SO2
SO2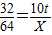 解得:X=20t
解得:X=20t 2CO2,CO2+C
2CO2,CO2+C 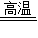 2CO,化合;(2)可燃物,①;(3)[实验探究1]II①硫,碳;②二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊;①证明煤中含有硫元素;②除去气体中的二氧化硫,避免对后面实验的干扰;③不变色,变浑浊;(4)10t.
2CO,化合;(2)可燃物,①;(3)[实验探究1]II①硫,碳;②二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊;①证明煤中含有硫元素;②除去气体中的二氧化硫,避免对后面实验的干扰;③不变色,变浑浊;(4)10t.

 阅读快车系列答案
阅读快车系列答案