
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
解答 解:活动性强的金属能把活动性弱的从它的盐溶液中置换出来,①A+B(NO3)2→A(NO3)2+B,说明A的金属活动性比B强,即A>B;②C+B(NO3)2→C(NO3)2+B,说明C的金属活动性比B强,即C>B;位于氢前面的金属能置换出酸中的氢,③A+H2SO4(稀)→ASO4+H2↑,说明A的金属活动性比氢强,即A>H;④C与H2SO4(稀)不反应,说明C的金属活动性比氢弱,即H>C.则三种金属的活动顺序是:A>C>B.
故答为:A>C>B.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
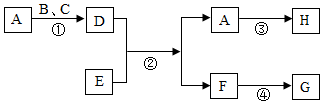 A-H是初中化学常见物质,其中D、H为红色固体,E为有毒气体,它们之间的转化关系如图所示,回答下列问题:
A-H是初中化学常见物质,其中D、H为红色固体,E为有毒气体,它们之间的转化关系如图所示,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com