
| 序 号 | 操 作 | 现 象 | 结 论 |
| 实验一 | 向氢氧化钡溶液中滴入酚酞 | 溶液变红 | 氢氧化钡溶液呈碱性 |
| 实验二 | 向实验一的溶液中通入 适量的二氧化碳 | 产生白色沉淀,红色消失 | 氢氧化钡溶液能与 二氧化碳反应 |
| 实验三 | 另取氢氧化钡溶液,滴入 一定量的碳酸钠溶液 | 产生白色沉淀 | 氢氧化钡溶液能与 碳酸钠溶液反应 |
| 序号 | 操作 | 现象 | 结论 |
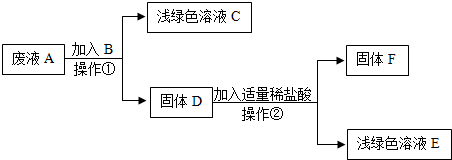
| 实验四 | 取滤液样品于试管中, 加入几滴稀盐酸 | 没有明显现象 | 猜想Ⅱ不成立 |
| 实验五 | 取滤液样品于试管中, 加入几滴碳酸钠溶液 | 有白色沉淀产生,红色不消失 | 猜想Ⅲ成立 |
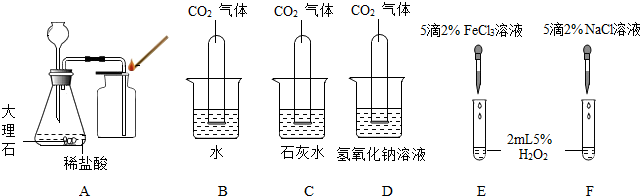
分析 实验一(1)据二氧化碳的实验室制取原理及可以从装置的漏气和气密性等方面分析原因解答;
(2)据二氧化碳的检验方法解答;
(3)据已知条件分析解答;
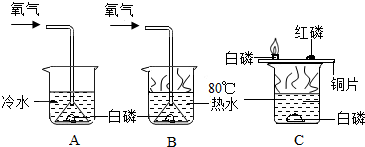
实验二(1)能证明可燃物必须达到一定温度(着火点)的变量是:温度,有冷水,有热水,有热水的必须能够燃烧,其它变量均相同,所以③④符合这一说法
(2)C装置在密闭环境中进行,避免了P2O5对空气的污染;
实验三(1)氢氧化钡与碳酸钠反应生成氢氧化钠和碳酸钡沉淀;
(2)碳酸钡与稀硫酸反应生成硫酸钡、水、二氧化碳;
(3)实验四取滤液样品于试管中,加入几滴稀盐酸,如果稀盐酸的量过少,则现象不明显;
(4)加入稀硫酸,如果只是红色消失,则证明有氢氧化钠,如红色消失,且有沉淀生成,则一定有氢氧化钡,如红色消失,且有气泡生成,则一定有碳酸钠.
(5)稀盐酸与碱完全反应溶液呈中性,酚酞试液显示无色.
解答 解:实验一(1)根据反应物是石灰石和盐酸,生成物是氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;装置的气密性都是经过检验的,观察装置看到长颈漏斗下端的管口与大气是相通的,生成的二氧化碳会从管口逸到空气中装置的气密性都是经过检验的,观察装置看到长颈漏斗下端的管口与大气是相通的,生成的二氧化碳会从管口逸到空气中
(2)B中发生反应的化学方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
(3)根据向下:E中产生大量气泡,F中没有明显现象分析,氯离子、钠离子不能使过氧化氢分解速度加快,所以是铁离子使双氧水分解的速率加快;
实验二(1)能证明可燃物必须达到一定温度(着火点)的变量是:温度,有冷水,有热水,有热水的必须能够燃烧,其它变量均相同,所以③④符合这一说法
(2)C装置在密闭环境中进行,避免了P2O5对空气的污染;
实验三(1)氢氧化钡与碳酸钠反应生成氢氧化钠和碳酸钡沉淀,反应的方程式为:Na2CO2+Ba(OH)2═BaCO3↓+2NaOH;
(2)碳酸钡与稀硫酸反应生成硫酸钡、水、二氧化碳,硫酸钡也是白色固体;
(3)实验四取滤液样品于试管中,加入几滴稀盐酸,如果稀盐酸的量过少,则现象不明显;
(4)加入稀硫酸,如果只是红色消失,则证明有氢氧化钠,如红色消失,且有沉淀生成,则一定有氢氧化钡,如红色消失,且有气泡生成,则一定有碳酸钠.
(5)稀盐酸与碱完全反应溶液呈中性,酚酞试液显示无色.
故答案为:实验一(1)CaCO3+2HCl═CaCl2+H2O+CO2↑、长颈漏斗未伸入液面,造成气体逸出;
(2)CO2+Ca(OH)2=CaCO3↓+H2O;
(3)Fe3+;
实验二(1)③④;(2)C装置在密闭环境中进行,避免了P2O5对空气的污染;
实验三(1)Na2CO2+Ba(OH)2═BaCO3↓+2NaOH;(2)硫酸钡也是白色固体;(3)稀硫酸;(5)红色消失.
点评 本题考查了学生利用题中信息结合已学知识探究分析问题的能力,只要认真分析,才能正确解答.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:初中化学 来源: 题型:多选题
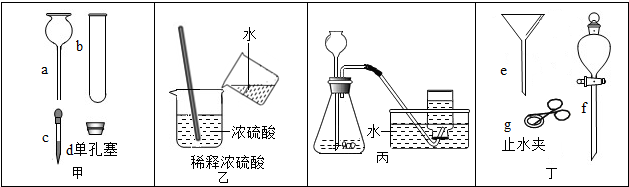
| A. | 将仪器a与d连接,可采用水湿润的办法,使a更易插入d中 | |
| B. | 图乙所示的操作不会造成液体飞溅 | |
| C. | 可利用装置丙丙制取二氧化碳实验 | |
| D. | 在图丙中为控制产生气体的速率,可先用图丁中的f代替图丙中的长颈漏斗 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | X的化学式为SO3 | |
| B. | 该反应是放热反应 | |
| C. | Na2S2O4需要干燥密闭储存 | |
| D. | 该反应中硫元素和氧元素的化合价都没有发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
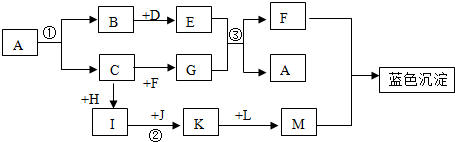
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 |  |  |  |
| (6.5~7.5) | (4.0~4.4) | (2.0~3.0) | (9.5~10.5) |
| A.饮用水 | B.番茄汁 | C.柠檬汁 | D.液体肥皂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
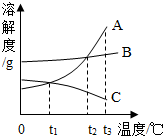 如图A、B、C三种物质的溶解度曲线,据图回答
如图A、B、C三种物质的溶解度曲线,据图回答查看答案和解析>>
科目:初中化学 来源: 题型:解答题
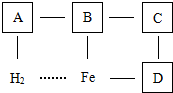 已知ABCD分别为H2SO4、NaOH、CuCl2和CuO中的一种.它们之间的关系如图所示(“--”表示能反应,“…”表示不能反应):
已知ABCD分别为H2SO4、NaOH、CuCl2和CuO中的一种.它们之间的关系如图所示(“--”表示能反应,“…”表示不能反应):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com