
向盛有10 mL稀盐酸(其中滴有少量紫色石蕊试液)的烧杯中加入NaOH溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下.请分析并回答下列问题:
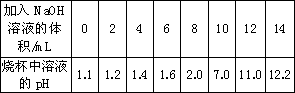
(1)当加入氢氧化钠溶液的体积为________mL时,稀盐酸和氢氧化钠溶液恰好完全反应.
(2)当加入氢氧化钠溶液的体积为13 mL时,溶液呈________色.
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?________.
科目:初中化学 来源: 题型:
| 加入碳酸钠溶液的体积/mL | 0 | 4 | 10 | 11 | 14 |
| 烧杯中溶液的pH | 1.1 | 4.3 | 7.0 | 8.4 | 12.2 |
查看答案和解析>>
科目:初中化学 来源:北京模拟题 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com