
分析 (1)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,然后依据质量守恒定律可以计算出第一次反应生成的氧气的质量;
(2)根据第一次反应生成氧气的质量可以计算出反应后剩余的高锰酸钾的质量;
(3)根据反应生成氧气的质量计算出生成物中二氧化锰的质量.
解答 解:(1)根据质量守恒定律可以知道第一次反应生成氧气的质量为:31.6g-30g=1.6g
两次反应生成氧气的质量为:1.6g+1.6g=3.2g
(2)设第一次反应消耗高锰酸钾的质量为x,生成二氧化锰的质量为y
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 87 32
x y 1.6g
$\frac{316}{x}$=$\frac{87}{y}$=$\frac{32}{1.6g}$
解得:x=15.8g y=4.35g
(2)第一次反应后剩余高锰酸钾的质量为:31.6g-15.8g=15.6g;
(3)实验结束后,可回收二氧化锰的质量为:4.35g×2=8.7g
答:(1)第一次反应生成氧气1.6克;两次反应共生成氧气3.2克;
(2)第一次反应后剩余高锰酸钾15.8g克;
(3)可回收二氧化锰的质量为8.7g克.
点评 本题主要考查学生对化学反应方程式的书写,以及运用方程式进行计算的能力.


科目:初中化学 来源: 题型:解答题
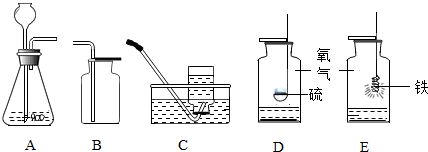
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钙用作食品干燥剂 | |
| B. | 浓硫酸露置于空气中,溶质质量分数变大 | |
| C. | 露置于空气中的固体氢氧化钠,其成分不会发生变化 | |
| D. | 打开浓盐酸的试剂瓶,瓶口会产生白雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 烧杯的质量/g | 18.2g |
| 烧杯及稀硫酸的质量/g | 33.2g |
| 铁钉(已用砂纸打磨去掉铁锈)/g | 10.8g |
| 反应后烧杯及所盛物质的总质量/g | 43.9g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
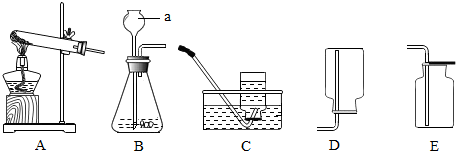
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
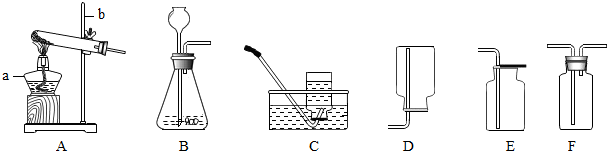
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作次序 | 第一次, | 第二次 | 第三次 | 第四次 |
| 剩余固体质量/g | 4.2 | 3.9 | 3.3 | 3.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
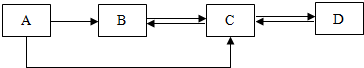
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com