
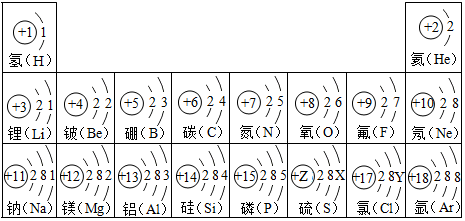
分析 (1)根据元素周期律:在元素周期表中,同一周期元素从左到右原子序数的逐渐递增;在原子中,原子序数=质子数=核外电子数;
(2)根据离子的形成以及离子符号的写法来分析;
(3)根据图中所给的信息及其规律进行解分析解答本题.
解答 解:(1)由元素周期律的特点可知同一周期元素从左到右原子序数的逐渐递增;故硫元素的核电荷数为16;根据在原子中,原子序数=质子数=核外电子数可知:氯元素的最外层电子数为17-2-8=7;故填:16;7;
(2)核电荷数为12的元素是镁元素,失去两个电子后形成的是镁离子;它的核外电子排布与氖元素的原子核外电子排布相同;故答案为:Mg2+;氖;
(3)图中的排列具有一定的规律,如:同一行中,从左到右元素的核电荷数依次递增.还能找到哪些规律有:同一行中最外层电子数依次递增(或同一列的最外层电子数相同)(其他答案合理也行).故答为:每一横行电子层数相等或每一纵行电子层数从上到下依次递增等.
点评 了解原子的构成特点,掌握了解元素周期表的特点和规律以及应用是解题的关键.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:初中化学 来源: 题型:选择题
| A. | 生活中可用煮沸的方法来降低水的硬度 | |
| B. | 进入久未开启的菜窖前,先用燃着的蜡烛进行实验 | |
| C. | 在室内放一盐水可以防止CO中毒 | |
| D. | 为了防止水体污染,要合理使用农药和化肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
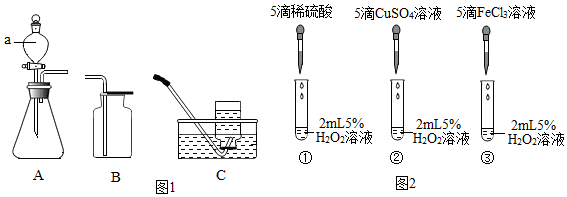
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用鼻子湊到容器口直接嗅闻未知气体的气味 | |
| B. | 用嘴品尝未知物质的味道 | |
| C. | 进入久未开启的菜窖、干涸的深井和深洞前,要做灯火试验 | |
| D. | 发现家里煤气泄漏时,应立即打开排气扇 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
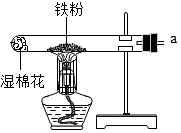 某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.| 操作方法 | 现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 维生素C中氧元素所占质量分数约为54.5% | |
| B. | 维生素C由碳、氢、氧三种元素构成 | |
| C. | 维生素C相对分子质量为176g | |
| D. | 维生素C分子是由6个碳原子、8个氢原子和6个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源:2017届四川省自贡市牛佛片区九年级综合素质模拟(二)化学试卷(解析版) 题型:信息分析题
请用化学用语表示。
(1)2个氯原子_________________(2)葡萄糖分子___________________
(3)铵根离子___________________(4)硫酸亚铁中的阳离子______________
(5)地壳中含量最多的金属元素________________
查看答案和解析>>
科目:初中化学 来源:2017届吉林省长春市九年级模拟化学试卷(解析版) 题型:信息分析题
金属镁可与热水反应生成氢氧化镁,所得溶液呈碱性,可使酚酞溶液显红色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
(1) 金属镁与热水反应的化学方程式为:____________ ;
(2) 溶液的红色褪去说明溶液的碱性;___________
(3) 据你推测,导致溶液碱性变化的原因是:①____________;②___________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com