
| 物质 | 番茄 | 肥皂水 | 牛奶 | 酱油 |
| pH | 4.0-4.4 | 9.5-10.5 | 6.3-6.6 | 4.0-5.0 |
| A. | 番茄 | B. | 肥皂水 | C. | 牛奶 | D. | 酱油 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
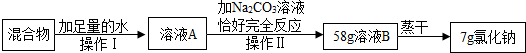
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
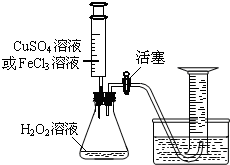 为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
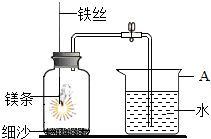 镁在充满空气中的集气瓶中燃烧,观察到的实验现象主要有发出耀眼的白光,放出大量的热,同时伴随有白烟产生,发反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,实验结束后经仔细观察,细心的同学发现了淡黄色固体,老师告诉大家这种淡黄色固体为Mg3N2,根据所学知识,空气中氮气和氧气的体积比为4:1,但镁条在空气中燃烧只生成少量的淡黄色固体,其原因是氧气的化学性质比氮气更活泼,镁条更易与氧气发生反应.
镁在充满空气中的集气瓶中燃烧,观察到的实验现象主要有发出耀眼的白光,放出大量的热,同时伴随有白烟产生,发反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,实验结束后经仔细观察,细心的同学发现了淡黄色固体,老师告诉大家这种淡黄色固体为Mg3N2,根据所学知识,空气中氮气和氧气的体积比为4:1,但镁条在空气中燃烧只生成少量的淡黄色固体,其原因是氧气的化学性质比氮气更活泼,镁条更易与氧气发生反应.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
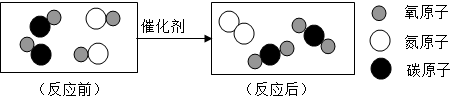
| A. | 该反应是复分解反应 | B. | 该反应中各元素化合价保持不变 | ||
| C. | 图中的化合物都属于氧化物 | D. | 该反应所得生成物质量之比为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
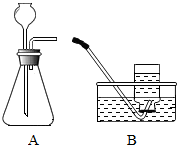 某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.| 编号 | 20%的稀硫酸各20mL | 锌粒 | 收集1瓶氢气所需的时间 |
| ① | 加入质量分数为10%的硫酸铜溶液1mL | 1g | 2分10秒 |
| ② | 加入质量分数为10%的硫酸锌溶液1mL | 1g | 3分01秒 |
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | 取1g锌粒于锥形瓶中, 加入20mL 20%的稀硫酸 | 产生氢气的速率较快与铜单质有关 | |
| ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com