
【题目】室温时,向氢氧化钠溶液中逐滴加入稀盐酸,符合右图中纵坐标X的表示是( )
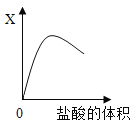
A.溶液的温度B.溶液中氯化钠的质量
C.溶液中含有HCl的物质的量D.溶液中氯化钠的质量分数
【答案】D
【解析】
A、盐酸和氢氧化钠溶液反应要放出热量,但开始的时候溶液的温度不应该为零,并且随着反应的开始和终止,溶液温度应该先升高后降低,故A错误;
B、氢氧化钠和盐酸反应生成了氯化钠,所以开始加入稀盐酸时即产生氯化钠,等把氢氧化钠消耗完全后氯化钠的质量不再增加,故B错误;
C、盐酸中溶质为氯化氢,而盐酸可以和氢氧化钠反应,所以表示氯化氢质量的起点不应该是原点,故C错误;
D、氢氧化钠和盐酸反应生成了氯化钠,开始溶液中氯化钠的质量分数为0,随着反应的进行,开始溶液中氯化钠的质量分数增大,完全反应时,溶液中氯化钠的质量分数最大,当盐酸过量时,溶液中氯化钠的质量分数减小,故正确.
故选D.


科目:初中化学 来源: 题型:
【题目】金属材料广泛用于生产生活中。三月莘县的街道上,出现了一排排“共享电单车”,作为代步工具,既轻便灵活又环保。
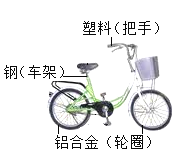
(1)所标部件中属于合成材料的是________。
(2)车架主要含有的金属元素是________(填名称);铝的化学性质比铁活泼,但空气中的铝却比铁耐锈蚀的主要原因是________。
(3)为了验证Mg、Fe、Cu三种金属的活动性顺序,下列选用的药品可行的是________(填序号)
①稀盐酸 ②MgSO4溶液、Fe、cu
③FeSO4溶液、Mg、Cu ④MgSO4溶液、FeSO4溶液、Cu
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某大理石样品(所含杂质不溶于水且不与酸反应)与足量的盐酸充分反应,过滤后将绿叶蒸干,冷却后称量所得氯化钙固体,相关实验数据如下图所示(不计损耗):
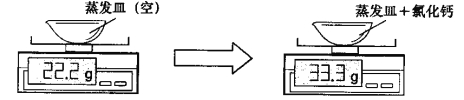
(1)氯化钙的质量为______________g。
(2)计算该大理石样品中碳酸钙的物质的量(根据化学方程式列式计算)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定量盐酸和氯化铜溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示.下列说法正确的是( )
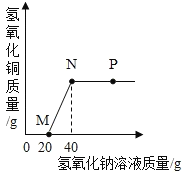
A.P点表示的溶液pH=7
B.N点表示的溶液中含有两种溶质
C.从M点到N点溶液质量增加20g
D.P点表示的溶液比N点表示的溶液中氯化钠的质量分数小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如下:
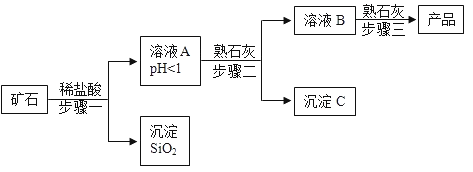
(1)溶液A中所含的阳离子有_______________(填离子符号)。
(2)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
步骤二中加入熟石灰,调节溶液的pH范围为______________。
(3)3个步骤中均用到的操作是_________________。
(4)步骤三中生成产品的化学方程式为___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
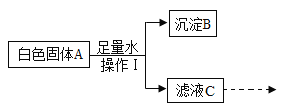
①操作I是____.
②在沉淀B中加入足量稀硝酸,沉淀部分溶解.根据上述实验分析,A中一定含有的物质是_____.写出沉淀部分溶解的化学方程式____.
③取少量滤液C于试管中,滴入酚酞,溶液变红,则C中一定含有的溶质是____.
④为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
实验操作 | 现象 | 结论 |
____ | ____ | 确定A固体中还含有氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示A、B两种固体物质的溶解度曲线:

(1)溶解度的单位是_____;当温度为_____℃时,A物质与B物质的溶解度相等。
(2)50℃时。20g水中加入_____g A物质,恰好得到饱和溶液。
(3)40℃时,如果A、B两种溶液的质量分数相等,该质量分数可以是_____(选填下列编号)。
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
(4)要将A物质从其溶液中结晶析出,采用蒸发结晶,理由是_____。
(5)如果A溶液中有少量的B杂质,为了得到较纯净的A,采用的方法是降温结晶而不采用蒸发结晶,理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草木灰可作肥料,同学取一些草木灰做了以下实验,请完成实验报告。
实验序号 | 实验目的 | 实验方案 | 实验现象 | 结论 | |
实验1 | 证明草木灰的主要成分含钾元素 | 取样,进行_________反应 | 透过蓝色钴玻璃片火焰呈__________色 | 草木灰主要成分含钾元素 | |
实验2 | _________ |
| _________ | 草木灰主要成分是碳酸钾 | |
实验3 | 探究碳酸钾性质 | 取样,向碳酸钾溶液中滴入石灰水溶液 | 生成白色沉淀 | 写反应化学方程式__________ | |
分析推测:实验3反应后上层清液中溶质成分组成____________________________ | |||||
实验4 | 探究实验3反应后上层清液中溶质成分 | 对实验3反应后的上层清液进行一次取样。 _________ | _________ | 反应后上层清液溶质成分是只含氢氧化钾 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某氢氧化钙中含有碳酸钙杂质,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡后形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,此时消耗盐酸的总质量为37.5g,锥形瓶中剩余物质的质量为80.3g。
(1)反应产生二氧化碳的质量为______g。
(2)求样品中氢氧化钙的质量分数_____(写出计算过程,结果精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com