
| 实验次数 | 一 | 二 | 三 | 四 |
| 固体混合物的质量(g) | 25 | 25 | 25 | 25 |
| 加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 1.45 | m | 4.35 | 4.35 |
分析 (1)根据加入20g氢氧化钠溶液质量得到沉淀1.45g,第三次实验加入60g氢氧化钠溶液生成沉淀增加了,说明第一次实验中20g氢氧化钠完全反应只能生成1.45g沉淀,加入40g氢氧化钠溶液质量是20g氢氧化钠溶液质量的2倍所以m值是1.45g的2倍;
(2)一切化学反应都遵循质量守恒定律;
(3)根据生成的总沉淀的质量计算出氯化镁的质量,用氯化镁的质量除以原固体混合物的质量,乘以百分之百即可.
解答 解:(1)根据加入20g氢氧化钠溶液质量得到沉淀1.45g,第三次实验加入60g氢氧化钠溶液生成沉淀增加了,说明第一次实验中20g氢氧化钠完全反应只能生成1.45g沉淀,加入40g氢氧化钠溶液质量是20g氢氧化钠溶液质量的2倍所以m值是1.45g的2倍,即为:2.9;故填:2.9;
(2)一切化学反应都遵循质量守恒定律;故填:是;
(3)设原固体混合物中MgCl2的质量为x
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 58
x 4.35g
$\frac{95}{58}=\frac{x}{4.35g}$
x=7.125g
原固体混合物中MgCl2的质量分数MgCl2%=$\frac{7.125g}{25g}$×100%=28.5%
答:原固体混合物中MgCl2的质量分数为28.5%
点评 解答本题关键是要分析m的值时找出加入氢氧化钠溶液的质量的关系,再推算出生成沉淀的质量


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:选择题
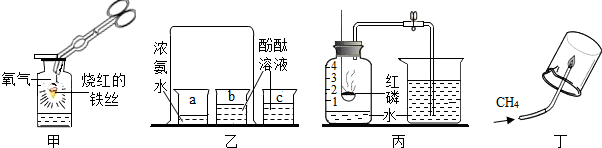
| A. | 甲:反应后集气瓶炸裂,是由于铁丝燃烧放热 | |
| B. | 乙:c烧杯的作用是验证空气中的物质不能使酚酞溶液变色 | |
| C. | 丙:进入瓶中的水约占瓶内原空气体积的$\frac{1}{5}$,是由于氧气约占空气体积的$\frac{1}{5}$ | |
| D. | 丁:烧杯内壁有水珠生成,说明甲烷中含有氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
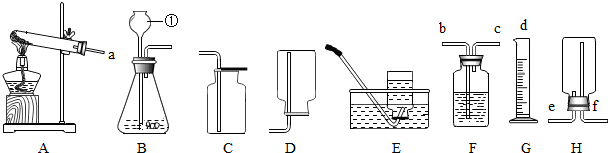
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe | B. | Ba(OH)2 | C. | CuO | D. | Cu(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  金属Metal | B. |  有害垃圾Harmful waste | ||
| C. |  可燃垃圾Combustible | D. |  玻璃Glass |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | a.测溶液pH | b.滴加Na2CO3溶液 | c.滴加BaC12溶液 |
| 实验操作 | 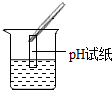 | 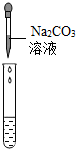 | 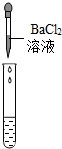 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 将一植物放在密闭的玻璃罩内,置于室外进行培养,用CO2浓度测定仪测得了该玻璃罩内CO2浓度的变化情况,绘成如图曲线,请据此回答:
将一植物放在密闭的玻璃罩内,置于室外进行培养,用CO2浓度测定仪测得了该玻璃罩内CO2浓度的变化情况,绘成如图曲线,请据此回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com