
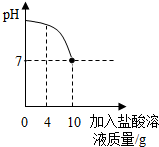
 实验室有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8g 10%的NaOH溶液.然后往烧杯中滴加该盐酸.反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:
实验室有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8g 10%的NaOH溶液.然后往烧杯中滴加该盐酸.反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:| 40 |
| 8g×10% |
| 36.5 |
| x |
| 0.73g |
| 10g |
| 23 |
| 40 |


科目:初中化学 来源: 题型:
| 药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
| 药品 | 盐酸、硫酸 | 氢氧化钠、氢氧化钙 | 红磷、硫 | 铜、锌 |
| A、甲柜 | B、乙柜 | C、丙柜 | D、丁柜 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 食品保鲜可以防止食品腐败,保持食品的营养和味道.食品保鲜的措施有添加防腐、充填气体、放置干燥剂或脱氧剂等.
食品保鲜可以防止食品腐败,保持食品的营养和味道.食品保鲜的措施有添加防腐、充填气体、放置干燥剂或脱氧剂等.
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com