
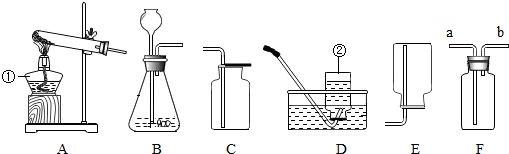
分析 (1)根据常用仪器的名称和用途分析解答;
(2)根据实验室制取气体的发生装置是由反应物的状态和反应条件决定的分析;根据实验室用氯酸钾和二氧化锰制取氧气的反应原理分析;根据排水法收集的氧气较为纯净分析;
(3)排水法量取气体体积气体应“浅入深出”,据此进行分析解答;
(4)据反应原理写出方程式,二氧化碳能使澄清的石灰水变浑浊,二氧化碳的密度比空气大解答;
(5)由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出所用盐酸中溶质的质量,再根据溶质质量分数的计算公式结合盐酸的溶质质量分数就能计算出盐酸的质量.
解答 解:(1)根据常用仪器可知①是酒精灯、②是集气瓶;
故答案为:酒精灯;集气瓶;
(2)实验室用氯酸钾和二氧化锰制取氧气属于固体加热反应制取气体,发生装置应选A;该反应的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;氧气的密度比空气大,不易溶于水,可用向上排空气法和排水法收集,但排水法收集的氧气较为纯净;
故答案为:A;2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2;D;
(3)气体应“浅入深出”,因此该气体应从b端进入F中;
故答案为:b;
(4)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;若用F装置收集,因二氧化碳的密度比空气大,二氧化碳应该从a进入;
故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O、a;
(5)解:设所用盐酸中溶质的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
x 6.6g
$\frac{73}{44}$=$\frac{x}{6.6g}$ x=10.95g
所用盐酸的质量为10.95g÷10%=109.5g
答:需要溶质的质量分数为10%的盐酸109.5g
点评 本题考查注重基础,主要考查了实验室制取气体的装置选取及实验和注意事项,难度不大.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
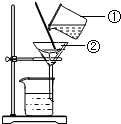 如图所示:
如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
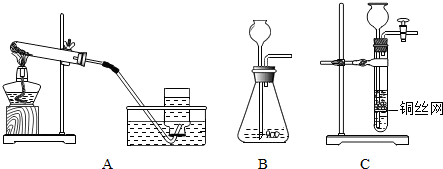
时间 浓度 条件 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com