
| A. | 分子 | B. | 原子 | C. | 元素 | D. | 单质 |
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:实验探究题
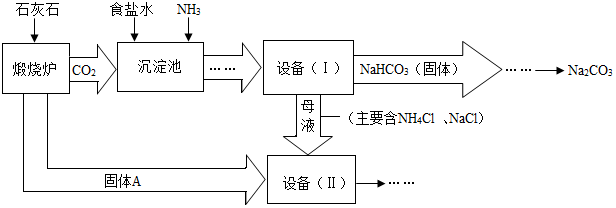
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
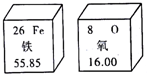
| A. | 氧原子的核外电子数为8 | |
| B. | 铁元素和氧元素都属于非金属元素 | |
| C. | 铁的相对原子质量是55.85g | |
| D. | 铁元素与氧元素只能组成一种化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题



查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的待测液于试管中,加入过量的氯化钙溶液. ②充分反应后静置,取上层淸液加入无色酚酞溶液 | 产生白色沉淀 无色酚酞溶液变红 | 猜想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
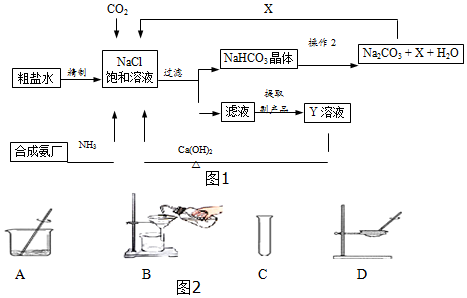
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 36.0 | 21.7 | 9.6 | 37.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com