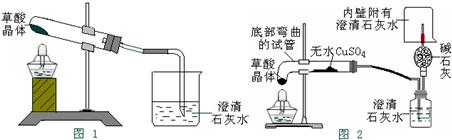
某研究性学习小组对双氧水开展如下研究.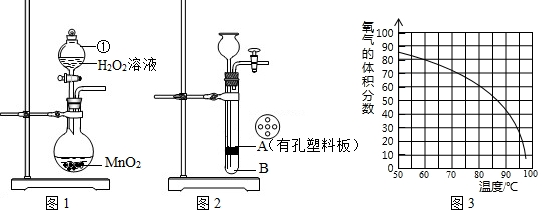
(1)图1装置中仪器①的名称为______.
(2)小林同学将MnO2与水泥按一定比例混合,制作成小块状固体,加入图2装置中制氧气以方便实验结束回收二氧化锰.其中块状固体应放置在______处(填“A”或“B”),二氧化锰的作用是______,该装置中反应的文字表达式是______.利用该装置反应一段时间后,需停止反应,其操作是______,原因是______.
(3)小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究.
第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、40%、50%的水.用排水法收集氧气,恰好把5只集气瓶中的水排去.将带火星的术条依次插入①~⑤号瓶中,记录实验现象.
小亮在前一组实验的基础上又做了第二组和第三组实验.三组实验的数据和现象见下表.
| 第一组 | 第二组 | 第三组 |
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
请根据实验回答下列问题:
①本实验中使用带火星的木条验满氧气的方法是否可靠:______(填“是”或“否”).
②收集的氧气占容积的体积分数最低为______%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数是______%(计算结果保留整数).
③用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸气所致,此时混合气体中氧气的体积分数随温度变化的曲线如图3所示.若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在______℃.


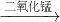 水+氧气;关闭活塞;关闭活塞后,产生的气体使试管中压强增大,液体被压回长颈漏斗中,固液分离,反应停止;
水+氧气;关闭活塞;关闭活塞后,产生的气体使试管中压强增大,液体被压回长颈漏斗中,固液分离,反应停止;

 53天天练系列答案
53天天练系列答案