
t℃时,某物质的溶液220g,蒸发去15g水后,析出晶体6g,又蒸发去10g水,析出6g晶体,再蒸去10g水又析出晶体的质量为
A.4g B.6g C.10g D.15g
B 【解析】 试题分析:t℃时,某物质的溶液220g,蒸发去15g水后,析出晶体6g,又蒸发去10g水,析出 6g晶体,由此可知,6g晶体溶解在10g水中形成饱和溶液,也就是说10g水中最多溶解6g该物质,由于析出晶体后的溶液是饱和溶液,所以将饱和溶液蒸发掉10g水析出晶体的质量应为6g.科目:初中化学 来源:江苏省苏州市2018届九年级上学期第一次月考 (1)化学试卷 题型:单选题
下列是今年无锡市实验操作考查“药品的取用和加热”中部分实验操作示意图。其中正确的是( )

A. A B. B C. C D. D
A 【解析】A.取用粉末状固体药品时,试管横放,然后用药匙将药品送入试管底部,然后慢慢竖起,故A正确;B.取用液体药品时应注意:①瓶塞倒放,防止沾的污物腐蚀瓶内的药品,②瓶口紧挨试管口,防止药品洒落,图中瓶塞没有倒放,试管没有倾斜,故B错误;C.给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的三分之一,图中液体超过试管容积的三分之一,故C错误;D.熄灭酒精灯...查看答案和解析>>
科目:初中化学 来源:广东省2018届九年级第一次模拟考试化学试卷 题型:简答题
下图是某品牌的保温瓶,请回答下列问题:

(1)该保温瓶的材质是不锈钢,请问不锈钢是___________(填“纯净物”或“混合物”)。
(2)不锈钢滤网相当于过滤实验中的______(填用名称)。
(3)醋酸(化学式:CH3COOH)和稀盐酸都具有酸的通性,是因为醋酸在水溶液中能电离出醋酸根离子(CH3COO-)和_______,请写出铁与醋酸反应生成醋酸亚铁((CH3COO)2Fe)与一种无色气体的反应方程式:________________________。
(4)制成合金是铁制品防锈的一种方法。为了防止铁制品生锈,除了将其制成合金,还可以__________________________(写出一种方法即可)达到防锈的目的。
混合物 滤纸 H+ 2CH3COOH + Fe = (CH3COO)2Fe + H2 ↑ 涂油(喷漆、搪瓷、电镀等) 【解析】本题考查了合金,金属与酸的反应和金属防锈措施等。 (1)不锈钢中含有铁、铬、镍,是混合物; (2)不锈钢滤网相当于过滤实验中的滤纸,能将固体与液体分离; (3)酸是由氢离子与酸根离子构成的化合物,所以醋酸在水溶液中能电离出CH3COO-和H+;铁与醋...查看答案和解析>>
科目:初中化学 来源:河北省南宫市2018届九年级上学期第二次月考化学试卷 题型:简答题
某兴趣小组要测定某石灰石样品中杂质的质量分数。他们进行了如图实验。(杂质不发生反应)
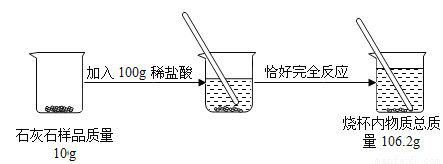
请计算:
(1)生成CO2气体的质量为________;
(2)样品中杂质的质量分数为________。
3.74g 15% 【解析】试题分析:根据质量守恒定律可知:反应后比反应前减少的质量即为反应放出二氧化碳气体的质量; 根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,从而可以求出样品中杂质的质量分数. (1)根据质量守恒定律,生成CO2气体的质量为:10g+100g-106.26g=3.74g; (2)【解析】 设石灰石中碳酸钙的质量为x 100 44 ...查看答案和解析>>
科目:初中化学 来源:河北省南宫市2018届九年级上学期第二次月考化学试卷 题型:单选题
向某无色溶液中加入氯化钡溶液,有白色沉淀产生,加入稀硝酸后白色沉淀不溶解,原溶液中
A. 一定含有SO42-
B. 一定含有Ag+
C. 含有SO42-和Ag+
D. 可能有SO42-或Ag+
D 【解析】某无色溶液加入氯化钡溶液后有白色沉淀,再加稀硝酸沉淀不消失,若原溶液中有Cl-,则会生成AgCl沉淀,若原溶液中有SO32-离子,则生成BaSO3沉淀,加稀硝酸,BaSO3沉淀被氧化为BaSO4沉淀,若溶液中有SO42-,则生成BaSO4沉淀,硫酸钡和氯化银都不溶于硝酸,所以原溶液中可能含有SO42-或SO32- 或Ag+。故选D。查看答案和解析>>
科目:初中化学 来源:河北省南宫市2018届九年级上学期第二次月考化学试卷 题型:单选题
为了防止铁制品受腐蚀,下列采取的措施中错误的是
A.保持铁制品表面的洁净和干燥
B.在铁制品表面涂上油
C.在铁制品表面镀上金属锌
D.把铁制品浸在水里使它与空气隔绝
D 【解析】 试题分析:防止金属生锈的原理是隔离氧气和水,具体的方法有:在金属表面涂一层油漆;在金属表面镀一层金属等. A.保持铁制品表面的洁净和干燥可以防止金属生锈; B.在铁制品表面涂上油,从而隔绝了氧气和水,可以防止金属生锈; C.在铁制品表面镀上金属锌可以防止金属生锈; D.因为水是铁生锈的条件之一,把铁制品浸在水里不能有效的防止铁生锈.查看答案和解析>>
科目:初中化学 来源:山东省济南市历下区2018届九年级中考三模化学试卷 题型:简答题
水及溶液与人类的生活生产密切相关。根据下列图示,请回答相关问题。
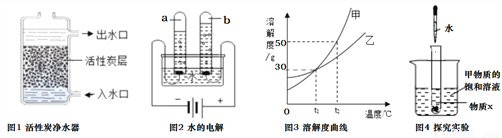
(1)图1中,活性炭净水器主要利用了活性炭具有的_______性;图2所示实验中,试管b中得到的气体是(写物质名称)_______。
②图3为甲、乙两种固体物质的溶解度曲线图。t1℃时,甲物质的溶解度是_________,t2℃时,甲的饱和溶液溶质质量分数_________乙的饱和溶液溶质质量分数(填“大于”、“等于”、“小于”之一);图4所示实验中,将水滴入盛有物质X的小试管中,可观察到烧杯中有甲物质的固体析出。则物质X可能是_________(填序号之一)。
A.食盐 B.烧碱 C.生石灰 D.硝酸铵
(3)海水中蕴着丰富的物物质资源。
①我国海盐年产量居世界第一位。目前从海水中提取食盐的方法主要为“盐田法”,生产流程如下图所示:
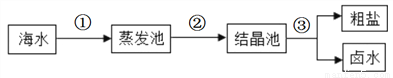
在蒸发池中促进水分蒸发,主要是利用了_________(填序号之一)。
A.潮沙汐能 B,生物能 C.电能 D.太阳能
上述流程中得到的卤水,是氯化钠的________溶液(填“饱和”或“不饱和”)。
②金属镁广泛应用于生活、生产和国防工业,从海水或卤水中提取镁的工艺流程如下图所示:
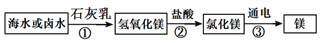
在上述转化过程,步骤①得到氢氧化镁固体的操作名称是___________,步骤②中发生反应的化学方程式为____________________________________。
吸附 氧气 30g 大于 D D 饱和 过滤 Mg(OH)2+2HCl=MgCl2+2H2O 【解析】(1)活性炭表面疏松多孔具有吸附性,由“正氧负氢”知,在正极上产生的气体是氧气,能吸附有色气体和异味;(2)由溶解度曲线可查出t1℃时硫酸钠的溶解度是30g;在t2℃时乙的溶解度曲线在甲的溶解度曲线下面,所以t2℃时乙的溶解度小于t2℃甲的溶解度,故甲的饱和溶液溶质质量分数大于乙的饱和溶液溶...查看答案和解析>>
科目:初中化学 来源:江苏省灌云县西片2018届九年级下学期第二次月考化学试卷 题型:综合题
某些食品的包装袋内,放有装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”。某同学对一袋久置空气中的干燥剂进行了探究。
他先取部分久置干燥剂倒入适量水中,充分搅拌、过滤,得到白色固体和滤液。然后对滤液的酸碱性和白色固体的组成作了探究。
(实验探究一)探究滤液的酸碱性
该同学测定了滤液的酸碱性,你认为该滤液显____________性。
(实验探究二)探究过滤后白色固体的组成
该同学认为白色固体中可能含有的物质是CaO、Ca(OH)2、CaCO3。
他查阅有关资料得知:CaO是一种白色固体,俗称生石灰,能与水反应生成氢氧化钙,并放出热量。氢氧化钙微溶于水。
(分析判断)你认为该过滤后得到的白色固体中一定不含有的物质是_______。
(实验操作)下面是该同学设计的进一步探究白色固体组成的实验方案,请你和他一起完成实验报告。
实验操作 | 实验现象 | 实验结论 |
①取少量白色固体,倒入适量水,充分搅拌、静置; ②向上层清液中滴加无色酚酞溶液 | 上层清液呈____色 | 白色固体中一定含有氢氧化钙 |
另取少量白色固体放入试管中,滴加稀盐酸 | _________ | 白色固体中一定含有碳酸钙 |
(总结反思)
只通过以上实验,还不能证明这袋久置于空气中的干燥剂中是否含有CaO。请你简述一个证明这袋干燥剂中含有较多量CaO的简易实验:____。用化学方程式表示其中的反应_____。
(实验探究三)探究干燥剂样品中碳酸钙的质量分数
取上述干燥剂样品10g放入如图的装置中,充分反应后,测出了量筒中的水的体积为220mL,(此状况下二氧化碳的密度是2g/L),则此干燥剂中碳酸钙的质量分数为___________(通过计算填空)
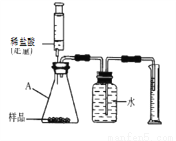
(总结反思)(实验探究三)中实验设计的不合理之处_________
碱性。 氧化钙或CaO 红 有气体产生 证明这袋干燥剂中含有较多量CaO的简易实验:取少量样品于试管中,加水溶解,触摸试管外壁,温度升高 CaO+H2O==Ca(OH)2 10% 生成的二氧化碳溶于水,与水发生反应,使二氧化碳的总体积减小 【解析】【实验探究一】如果久置的干燥剂中含有氧化钙,或含有氢氧化钙,或含有氧化钙和氢氧化钙,倒入适量水中,充分搅拌、过滤后的滤液中含有氢氧化钙,滤液显碱性...查看答案和解析>>
科目:初中化学 来源:四川省安岳县2017届九年级上学期期末考试理科综合化学试卷 题型:简答题
鸡蛋壳的主要成分是碳酸钙,其余为杂质,(杂质不溶于水且不参加反应)为了测定蛋壳中碳酸钙的质量分数。小东和小明同学进行了如下实验,相关实验数据如下图所示:
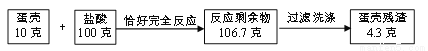
(1)小东根据“蛋壳残渣质量为4.3克”,求得蛋壳中碳酸钙的质量分数为_________;
(2)小明根据“反应过程中减少的质量”(10克+100克-106.7克=3.3克)也求得了蛋壳中碳酸钙的质量分数,请你写出小明的计算过程和结果__________________。
(3)小东和小明经过反复实验得出该鸡蛋壳中碳酸钙的质量分数与小明结果吻合,请分析小东开始所得结果出现误差的原因是__________________________。
57% 75% 小东计算所用的蛋壳残渣未干燥 【解析】(1)小东根据“蛋壳残渣质量为4.3克”,求得蛋壳中碳酸钙的质量分数为(10g-4.3g)÷10g×100%=57%;(2)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,所以生成二氧化碳的质量=参加反应前各物质的质量总和反应后剩余各物质的质量总和;生成二氧化碳的质量为:10g+100g-106....查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com