将混有CaCl2的食盐25g放入173g水中,完全溶解后,再加入溶质的质量分数为20%的Na2CO3溶液53g,恰好完全反应.试求:
(1)原食盐中混有CaCl2的质量.
(2)反应所得溶液中的溶质质量分数.
【答案】
分析:(1)根据碳酸钠与氯化钙反应的化学方程式和碳酸钠的质量,列出比例式,就可计算出原食盐中混有CaCl
2的质量和反应生成NaCl的质量;
(2)反应所得溶液中的溶质质量=混合物质量-混有CaCl
2的质量+生成NaCl的质量,反应后所得溶液的质量=混合物质量+水的质量+碳酸钠溶液质量-生成沉淀的质量,然后根据溶质质量分数=

计算即可.
解答:解:(1)设原食盐中混有CaCl
2的质量为x,反应生成NaCl的质量为y,
CaCl
2+Na
2CO
3═CaCO
3↓+2NaCl
111 106 117
x 53g×20% y
∴
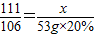
,
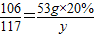
解之得:x=11.1g,y=11.7g.
(2)反应所得溶液中的溶质质量=25g-11.1g+11.7g=25.6g,
生成沉淀的质量为:11.1g+53g×20%-11.7g=10g,
反应后所得溶液的质量为:25g+173g+53g-10g=241g,
反应所得溶液中的溶质质量分数为:
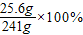
≈10.6%.
答:(1)原食盐中混有CaCl
2的质量为11.1g;
(2)反应所得溶液中的溶质质量分数为10.6%.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.

 计算即可.
计算即可.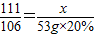 ,
,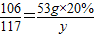
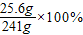 ≈10.6%.
≈10.6%.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案