
 铁是应用最广泛的金属,因此铁及其化合物是中学化学学习和研究的重要内容.
铁是应用最广泛的金属,因此铁及其化合物是中学化学学习和研究的重要内容.分析 (1)根据元素周期表一个格的含义分析回答.
(2)根据质量守恒定律分析X的化学式.
(3)根据化合价原则求出高铁酸钾(K2FeO4)中铁元素的化合价.
(4)根据铁生锈的条件及除锈的原理分析回答.
(5)根据金属活动性顺序表的应用分析判断.
(6)由铁的质量,根据赤铁矿炼铁的化学方程式可以列式计算出需要氧化铁质量分数为80%的赤铁矿石的质量.
解答 解(1)由元素周期表中一个格的含义可知,其中A表示相对原子质量.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2X↑+4H2O,反应前铜、氢、氮、氧原子个数分别为3、8、8、24,反应后的生成物中铜、氢、氮、氧原子个数分别为3、8、6、22,根据反应前后原子种类、数目不变,则2X分子中含有2个氮原子和2个氧原子,则每个X分子由1个氮原子和1个氧原子构成,则物质X的化学式为NO.
(3)设高铁酸钾(K2FeO4)中铁的化合价为x,则(+1)×2+x+(-2)×4=0,解得x=+6;
(4)铁锈的主要成分是氧化铁,能与盐酸反应生成了氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.铁制品生锈会给生产、生活带来诸多不便和危害,但事物都是一分为二的,冬天常用的防寒用品--“暖宝宝”却是利用铁与氧气、水 等反应生锈原理放出的热量为人类服务.
(5)由于金属的活动性顺序是铁>铜>银,将铁粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,铁先与AgNO3反应生成了硝酸亚铁和银,当AgNO3反应完全后,铁再与硝酸铜反应,生成了硝酸亚铁和铜.
①若滤液中只含一种溶质,该溶质是硝酸亚铁,滤渣的成分滤渣中一定含有Cu和Ag,可能含有Fe.
②若滤渣中含有两种金属,该金属是银和铜,滤液的成分滤液中一定含有Fe(NO3)2,可能含有Cu(NO3)2.
(6)设所需赤铁矿的质量为x
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2
160 112
x×80% 112t
$\frac{160}{112}=\frac{x×80%}{112t}$ 解得 x=200t
故答为:(1)相对原子质量;(2)NO;(3)+6;(4)Fe2O3+6HCl═2 FeCl3+3H2O;氧气、水;
(5)①滤渣中一定含有 Cu和Ag,可能含有Fe.②滤液中一定含有Fe(NO3)2,可能含有 Cu(NO3);(6)200t.
点评 本题较为全面地考查了有关铁的知识,难度不大,加强有关铁的知识的归纳和学习有利于解答本类题.


科目:初中化学 来源: 题型:选择题
| A. | 门捷列夫用定量的方法研究空气的成分 | |
| B. | 生活中可以用煮沸的方法降低水的硬度 | |
| C. | 我国的纯碱资源比较丰富、用纯碱来制取大量食盐 | |
| D. | 发现厨房燃气泄漏时,立即打开排风扇电源开关 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
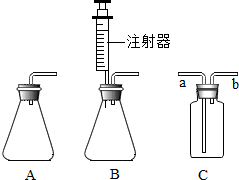 某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用A装置来制取氧气.
某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用A装置来制取氧气.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
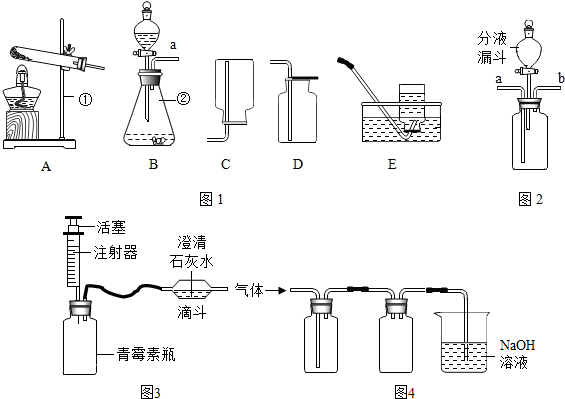
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 检验CO2气体 | 用燃着的小木条放在集气瓶口 |
| B | 除去CuO中混有的少量Cu | 加过量的稀盐酸,充分反应后过滤 |
| C | 除去NaN03溶液中混有的少量NaCl | 加过量AgN03溶液,充分反应后过滤 |
| D | 区分硝酸铵和尿素 | 加熟石灰研磨,闻气味 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
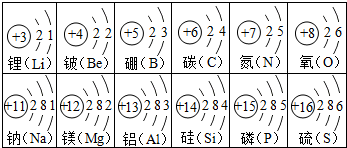 如图是部分元素的原子结构示意图,请回答:
如图是部分元素的原子结构示意图,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 往纯碱溶液中加入足量稀盐酸产生无色气体 | |
| B. | 磷在氧气中燃烧产生明亮的蓝紫色火焰 | |
| C. | 把面粉放入热水中搅拌后形成澄清透明的溶液 | |
| D. | 往烧碱溶液中滴入稀硫酸生成白色难溶物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com