
 Ϊ�˲ⶨij�ֻ�ͭ��ͭ��п�ĺϽ𣩵���ɣ���ȡ�û�ͭ��Ʒ��м100g����400gϡ�����4�μ��뵽����Ʒ�У�������ݼ�¼���±�����Zn+H2SO4�TH2��+ZnSO4��
Ϊ�˲ⶨij�ֻ�ͭ��ͭ��п�ĺϽ𣩵���ɣ���ȡ�û�ͭ��Ʒ��м100g����400gϡ�����4�μ��뵽����Ʒ�У�������ݼ�¼���±�����Zn+H2SO4�TH2��+ZnSO4��| ��1�� | ��2�� | ��3�� | ��4�� | |
| ����ϡ����������g�� | 100 | 100 | 100 | 100 |
| ʣ�����������g�� | 87 | 74 | 67.5 | 67.5 |
���� п��ϡ���ᷴӦ��������п�����������ݷ�Ӧ�Ļ�ѧ����ʽ�����ṩ�����ݿ��Խ�����ط���ļ�����жϣ�
��� �⣺��1����3�μ���ϡ��������������Ȼ��С��˵����2�η�Ӧ���������Ȼ����п�����ʣ�����ijɷ��к���ͭ��п��
���ͭ��п��
��2���û�ͭ��Ʒ��ͭ��п���������ǣ�67.5g����100g-67.5g��=27��13��
���27��13��
��3����1����13gп��100gϡ����ǡ����ȫ��Ӧ���跴Ӧ����������Ϊx��
Zn+H2SO4�TZnSO4+H2����
65 98
13g x
$\frac{65}{13g}$=$\frac{98}{x}$��
x=19.6g��
����ϡ�����������������Ϊ��$\frac{19.6g}{100g}$��100%=19.6%��
������ϡ�����������������Ϊ19.6%��
������������������Ϊy��ǡ����ȫ��Ӧʱ������������Ϊz��
ͭ����Ϊ��100g-67.5g=32.5g��
Zn+H2SO4�TZnSO4+H2����
65 98 2
32.5g z y
$\frac{65}{100g-67.5g}$=$\frac{98}{z}$=$\frac{2}{y}$��
y=1g��z=49g��
ǡ����ȫ��Ӧ����ϡ��������Ϊ��49g��19.6%=250g��
��Ӧ���ɵ��������������ϡ���������Ĺ�ϵͼ����ͼ��ʾ��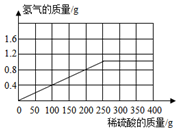
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ������Ӻ���ԭ�ӹ��� | B�� | ���ǵ�ˮ�����˺�͵õ�������ˮ | ||
| C�� | ��ˮ���ɵķ�Ӧһ�����кͷ�Ӧ | D�� | ��ˮ���Լ���̼��ƺ�̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ڢ� | C�� | �ڢۢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢޢ� | B�� | �٢ڢۢ� | C�� | �ۢݢޢ� | D�� | �ܢݢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ྻ�Ŀ��� | B�� | Һ̬�� | C�� | ��ˮ | D�� | ˮ��ɰ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
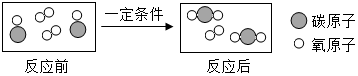
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ�����ƶ�����̼��CaCO3+H2SO4=CaSO4+H2O+CO2�� | |
| B�� | ʵ������������H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2��+O2�� | |
| C�� | ʵ������������Zn+2HCl=ZnCl2+H2�� | |
| D�� | ʵ����ģ��������3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com