
”¾ĢāÄæ”æ”°Ėį”¢¼īŗĶŃĪµÄČܽāŠŌ±ķ£ØŹŅĪĀ£©”±ŹĒѧĻ°»ÆѧµÄÖŲŅŖ¹¤¾ß£¬ÖĒ»ŪŠ”×éĶ¬Ń§ĄūÓĆøĆ¹¤¾ß½ųŠŠĢ½¾æѧĻ°”£
Ģ½¾æ»ī¶ÆŅ»£ŗČĻŹ¶¹¤¾ß
ČēĻĀĶ¼£¬±ķÖŠ±ź×¢ĮĖ¼×”¢ŅŅ”¢±ū”¢¶”ŗĶĪģĪåÖÖĪļÖŹ£¬ĪļÖŹµÄČܽāŠŌ¾łĪ“±źĆ÷”£
²æ·ÖĖį”¢¼īŗĶŃĪµÄČܽāŠŌ±ķ£ØŹŅĪĀ£©
ŅõĄė×Ó ŃōĄė×Ó | OH£ | NO3£ | Cl£ | SO42£ | CO32£ |
K£« | ¼× | ŅŅ | ±ū | ||
Ba2£« | ¶” | Īģ |
£Ø1£©ČĻŹ¶·ūŗÅ£ŗNO3£Ćū³ĘŹĒ___________£»
£Ø2£©Š“»ÆѧŹ½£ŗ±ūĪļÖŹµÄ»ÆѧŹ½ŹĒ_______________£»
£Ø3£©ĪļÖŹ·ÖĄą£ŗĪåÖÖĪļÖŹÖŠ£¬ŹōÓŚ¼īµÄŹĒ__________£ØÓĆ»ÆѧŹ½±ķŹ¾£©£»
£Ø4£©ČܽāÄÜĮ¦£ŗĪåÖÖĪļÖŹÖŠ£¬Ö»ÓŠŅ»ÖÖ²»ČÜÓŚĖ®£¬ĖüŹĒ____________£ØÓĆ»ÆѧŹ½±ķŹ¾£©”£
Ģ½¾æ»ī¶Æ¶ž£ŗŌĖÓĆ¹¤¾ß
ÓŠŅ»°ü°×É«·ŪÄ©æÉÄÜŗ¬ÓŠĀČ»Æ±µ”¢Ģ¼Ėį±µ”¢Ģ¼ĖįÄĘ”¢ĒāŃõ»ÆÄĘŗĶĮņĖįÄĘÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£¬Č”Ņ»¶ØĮæøĆ·Ūĩѳʷ¼ÓČėµ½Ź¢ÓŠ×ćĮæĖ®µÄÉÕ±ÖŠ£¬½Į°č£¬¾²ÖĆ£¬¹Ū²ģµ½ÉÕ±ÖŠÓŠ°×É«²»ČÜĪļ£¬Š”Ö£Ķ¬Ń§½«ÉÕ±ÖŠµÄĪļÖŹ¹żĀĖ£¬µĆĀĖŌüAŗĶĀĖŅŗB£¬Č”ĀĖŌüAÓŚŹŌ¹ÜÖŠµĪ¼Ó¹żĮæĻ”ĻõĖį£¬¹Ū²ģµ½ĀĖŌüČ«²æČܽā£¬ÓŠĘųÅŻ²śÉś”£
Š”ŃīĶ¬Ń§½ųŅ»²½Éč¼ĘĮĖČēĻĀŹµŃé·½°ø£¬Č·¶Ø°×É«·ŪÄ©µÄ×é³É£ŗ

Õė¶ŌÉĻŹöŹµŃé·½°øÖŠø÷²½ÖčµÄĻÖĻ󣬊”ŃīĶ¬Ń§Ģį³öĻĀĮŠČżÖÖ²»Ķ¬µÄ¼ŁÉč£¬ŅĄ¾ŻĆæÖÖ¼ŁÉčÖŠø÷²½Öč²»Ķ¬µÄŹµŃéĻÖĻó£¬æÉµĆ³ö²»Ķ¬µÄŹµŃé½įĀŪ”£
²½ÖčŅ» | ²½Ö趞 | ²½ÖčČż | |
¼ŁÉčŅ» | ÓŠ°×É«³ĮµķÉś³É | ||
¼ŁÉ趞 | ĪŽ°×É«³ĮµķÉś³É | ČÜŅŗ±äŗģ | ČܱäĪŖĪŽÉ« |
¼ŁÉčČż | ĪŽ°×É«³ĮµķÉś³É | ĪŽĆ÷ĻŌĻÖĻó | ĪŽĆ÷ĻŌĻÖĻó |
£Ø1£©ŅĄ¾Ż¼ŁÉčŅ»µÄĻÖĻó£¬æÉČ·¶ØŌ°×É«·ŪÄ©ÖŠÖ»ŗ¬ÓŠĢ¼Ėį±µ”¢Ģ¼ĖįÄĘ”¢ĒāŃõ»ÆÄĘŗĶĮņĖįÄĘĖÄÖÖĪļÖŹ”£Ōņ²½Ö趞µÄĻÖĻóŹĒ____________£»²½ÖčČżµÄĻÖĻóŹĒ_____________£»²½ÖčČżÖŠ·¢ÉśµÄČĪŅāŅ»øö»Æѧ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_________________”£
£Ø2£©ŅĄ¾Ż¼ŁÉ趞µÄĻÖĻó£¬Ō°×É«·ŪÄ©æÉÄܵÄ×é³ÉŹĒ_______________£»£ØČĪŠ“Ņ»ÖÖæÉÄܵÄ×é³É£¬ÓĆ»ÆѧŹ½±ķŹ¾£©
£Ø3£©ŅĄ¾Ż¼ŁÉčČżµÄĻÖĻó£¬Ō°×É«·ŪÄ©æÉÄܵÄ×é³ÉÓŠ___________ÖÖ”£
”¾“š°ø”æ ĻõĖįøł K2SO4 KOH BaCO3 ČÜŅŗÓÉĪŽÉ«±ä³ÉŗģÉ« ČÜŅŗÓÉŗģÉ«±ä³ÉĪŽÉ«£¬ÓŠĘųÅŻ²śÉś£¬³Įµķ²æ·ÖČܽā BaCO3 + 2HNO3 = Ba(NO3)2 + H2O + CO2”ü »ņNaOH + HNO3 = NaNO3 + H2O NaOH BaCO3
£»NaOH BaCl2 Na2CO3£»NaOH BaCl2 BaCO3£»NaOH BaCO3 Na2CO3 BaCl2£ØČĪŠ“Ņ»ÖÖæÉÄܵÄ×éŗĻ£© 4
”¾½āĪö”æĢ½¾æ»ī¶ÆŅ»£ŗ(1)NO3£Ćū³ĘŹĒĻõĖįøłĄė×Ó£»(2)ÓÉK+æÉµĆ¼ŲŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+1¼Ū£¬SO42£æɵĆĮņĖįøłµÄ»ÆŗĻ¼ŪĪŖ-2¼Ū£¬ÓÉĮ½Į£×Ó½įŗĻŠĪ³ÉĪļÖŹµÄ»ÆѧŹ½ŹĒ£ŗK2SO4£»(3)¼īŹĒÖøµēĄėŹ±Éś³ÉµÄŅõĄė×ÓČ«²æŹĒĒāŃõøłĄė×ӵĻÆŗĻĪļ£¬ĖłŅŌĪåÖÖĪļÖŹÖŠ£¬ŹōÓŚ¼īµÄŹĒ¼×£ØĒāŃõ»Æ¼Ų£©»ÆѧŹ½ĪŖ£ŗKOH£»(4)Ģ¼Ėį±µ²»ČÜÓŚĖ®£¬»ÆѧŹ½ĪŖ£ŗBaCO3£»Ģ½¾æ»ī¶Æ¶ž£ŗĢ¼Ėį±µÄŃČÜÓŚĖ®£¬ČÜÓŚĖį£¬Ģ¼ĖįÄĘŗĶĀČ»Æ±µ·“Ӧɜ³ÉČÜÓŚĖįµÄĢ¼Ėį±µ³Įµķ£¬ĮņĖįÄĘŗĶĀČ»Æ±µ·“Ӧɜ³É²»ČÜÓŚĖįµÄĮņĖį±µ³Įµķ£¬ĖłŅŌ£ŗČ”Ņ»¶ØĮæøĆ·Ūĩѳʷ¼ÓČėµ½Ź¢ÓŠ×ćĮæĖ®µÄÉÕ±ÖŠ£¬½Į°č£¬¾²ÖĆ£¬¹Ū²ģµ½ÉÕ±ÖŠÓŠ°×É«²»ČÜĪļ£¬Š”Ö£Ķ¬Ń§½«ÉÕ±ÖŠµÄĪļÖŹ¹żĀĖ£¬µĆĀĖŌüAŗĶĀĖŅŗB£¬Č”ĀĖŌüAÓŚŹŌ¹ÜÖŠµĪ¼Ó¹żĮæĻ”ĻõĖį£¬¹Ū²ģµ½ĀĖŌüČ«²æČܽā£¬ÓŠĘųÅŻ²śÉś£¬ĖłŅŌ·ŪÄ©ÖŠŅ»¶Ø²»ŗ¬ĮņĖįÄĘ£¬²»ČÜĪļæÉÄÜŹĒŌÓŠµÄĢ¼Ėį±µ£¬æÉÄÜŹĒĀČ»Æ±µŗĶĢ¼ĖįÄĘ·“Ӧɜ³ÉĢ¼Ėį±µ£¬»¹æÉÄÜŗ¬ÓŠĒāŃõ»ÆÄĘ£¬ĖłŅŌČÜŅŗBÖŠæÉÄÜŗ¬ÓŠĀČ»Æ±µ»ņĢ¼ĖįÄĘÖŠµÄŅ»ÖÖ£¬Ņ²æÉÄÜŗ¬ÓŠĮņĖįÄĘ£¬ĒāŃõ»ÆÄĘ£¬ĖłŅŌ£ŗ(1)ŅĄ¾Ż¼ŁÉčŅ»µÄĻÖĻó£¬æÉČ·¶ØŌ°×É«·ŪÄ©ÖŠÖ»ŗ¬ÓŠĢ¼Ėį±µ”¢Ģ¼ĖįÄĘ”¢ĒāŃõ»ÆÄĘŗĶĮņĖįÄĘĖÄÖÖĪļÖŹ£¬Ģ¼ĖįÄĘ”¢ĒāŃõ»ÆÄĘŌŚČÜŅŗÖŠĻŌ¼īŠŌ£¬Ģ¼ĖįÄĘŗĶĻ”ĻõĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼ĘųĢ壬ĖłŅŌ²½Ö趞µÄĻÖĻóŹĒČÜŅŗ±äŗģÉ«£»²½ÖčČżµÄĻÖĻóŹĒ£ŗÓŠĘųÅŻ²śÉś£»²½ÖčČżÖŠ·¢ÉśµÄ·“Ó¦ÓŠĒāŃõ»ÆÄĘŗĶĻõĖį·“Ӧɜ³ÉĻõĖįÄĘŗĶĖ®£¬»Æѧ·½³ĢŹ½ŹĒ£ŗNaOH+HNO3=NaNO3+H2O£»(2)¼ÓČė¹żĮæµÄĻõĖį±µ£¬ĪŽ°×É«³ĮµķÉś³É£¬ĖłŅŌBÖŠŅ»¶Ø²»ŗ¬ĮņĖįÄĘ”¢Ģ¼ĖįÄĘ£¬µĪČė·ÓĢŖ£¬ČÜŅŗ±äŗģÉ«£¬BÖŠæÉÄÜŗ¬ÓŠĢ¼ĖįÄĘ»ņĒāŃõ»ÆÄĘ£¬µĪ¼ÓĻõĖį£¬ČÜŅŗĶŹÉ«£¬ĖłŅŌČÜŅŗBÖŠŅ»¶Øŗ¬ÓŠĒāŃõ»ÆÄĘ£¬ĖłŅŌŌ°×É«·ŪÄ©æÉÄܵÄ×é³ÉŹĒ£ŗNaOH”¢BaCO3£»(3)¼ÓČė¹żĮæµÄĻõĖį±µ£¬ĪŽ°×É«³ĮµķÉś³É£¬ĖłŅŌBÖŠŅ»¶Ø²»ŗ¬ĮņĖįÄĘ”¢Ģ¼ĖįÄĘ£¬µĪČė·ÓĢŖ£¬Ć»ÓŠĆ÷ĻŌĻÖĻó£¬BÖŠ²»ŗ¬ÓŠĢ¼ĖįÄĘ»ņĒāŃõ»ÆÄĘ£¬µĪ¼ÓĻõĖį£¬Ć»ÓŠĆ÷ĻŌĻÖĻó£¬ĖłŅŌČÜŅŗBÖŠŅ»¶Ø²»ŗ¬Ģ¼ĖįÄĘ£¬ĖłŅŌŌ°×É«·ŪÄ©æÉÄܵÄ×é³ÉÓŠ£ŗĢ¼Ėį±µ”¢ĮņĖįÄĘ£¬Ģ¼Ėį±µ”¢ĀČ»Æ±µ£¬Ģ¼Ėį±µ”¢ĀČ»Æ±µ”¢Ģ¼ĖįÄĘ£¬Ģ¼ĖįÄĘ”¢ĮņĖįÄĘĖÄÖÖ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ 1 ĖłŹ¾ŹĒŹµŃéŹŅÖĘČ”ŃõĘųµÄ×°ÖĆĶ¼£¬Ēė°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā
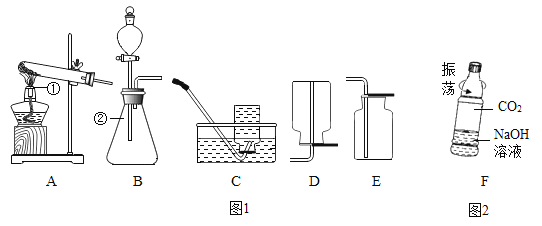
(1)Š“³öĶ¼ÖŠ±źŗÅŅĒĘ÷µÄĆū³Ę£ŗ¢Ł____£¬¢Ś_____”£
(2)ŹµŃéŹŅÓĆĀČĖį¼ŲÖĘČ”²¢ŹÕ¼ÆŅ»ĘæøÉŌļµÄŃõĘų£¬Ó¦Ń”ÓƵÄ×°ÖĆ×éŗĻŹĒ_____(Ģī×ÖÄøŠņŗÅ)
(3)ÓĆĀČĖį¼ŲŗĶ¶žŃõ»ÆĆĢÖʱøŃõĘųŹ±£¬¶žŃõ»ÆĆĢŌŚ·“Ó¦ÖŠµÄ×÷ÓĆŹĒ_______£¬ ĄūÓĆĻĀĮŠĮ÷³Ģ·ÖĄė²¢»ŲŹÕ³ä·Ö·“Ó¦ŗóµÄŹ£Óą¹ĢĢ壬Ēė»Ų“šĻĀĮŠĪŹĢā
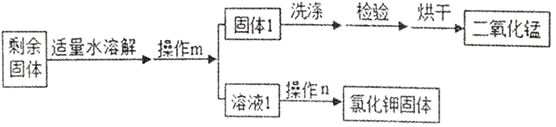
²Ł×÷ m µÄĆū³ĘŹĒ_______ £¬²Ł×÷ m ŗĶ²Ł×÷ n ÖŠ¶¼ÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ________£»
(4)Źµ Ńé ŹŅ ÓĆ ŃĪ Ėį ŗĶ Ģ¼ Ėį øĘ ÖĘ ¶ž Ńõ »Æ Ģ¼ £¬ øĆ ·“ Ó¦ µÄ »Æ ѧ ·½ ³Ģ Ź½ ĪŖ _________ £»ÓĆĶ¼ 2 ÖŠ F ĖłŹ¾µÄæóČŖĖ®Ęæ½ųŠŠ¶Ō±ČŹµŃ飬æÉ ŅŌÖ¤Ć÷ CO2 Óė NaOH ČÜŅŗČ·Źµ·¢ÉśĮĖ·“Ó¦£¬Ó¦×öµÄ¶Ō±ČŹµŃéŹĒ_______£»CO2 Óė NaOH ČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖÕÖŻŹ¢²śŃīĆ·”£ŃīĆ·ÖŠŗ¬ÓŠ·įø»µÄŅ¶Ėį£¬¶Ō·Ą°©æ¹°©ÓŠ»ż¼«×÷ÓĆ£¬Ęä»ÆѧŹ½ĪŖCl9Hl9N7O6”£ĻĀĮŠÓŠ¹ŲŅ¶ĖįµÄĖµ·ØÖŠÕżČ·µÄŹĒ
A£®Ņ¶ĖįµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ441 g
B£®Ņ¶ĖįÖŠµŖŌŖĖŲµÄÖŹĮæ·ÖŹż“óÓŚŃõŌŖĖŲµÄÖŹĮæ·ÖŹż
C£®Ņ¶ĖįÖŠĢ¼”¢Ēā”¢µŖ”¢ŃõĖÄÖÖŌŖĖŲÖŹĮæ±ČĪŖ19£ŗ19£ŗ7£ŗ6
D£®Ņ¶ĖįÓÉ19øöĢ¼Ō×Ó”¢19øöĒāŌ×Ó”¢7øöµŖŌ×ÓŗĶ6øöŃõŌ×Ó¹¹³É
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ŖŃ©Ķ¬Ń§¶ŌĀČ»ÆĆ¾¹ĢĢåѳʷ£Ø½öŗ¬ŌÓÖŹNaCl£©½ųŠŠČēĻĀ¼ģ²ā£ŗČ”5£®0gѳʷČÜÓŚŅ»¶ØĮæµÄĖ®ÖŠµĆµ½25£®0gČÜŅŗ£¬ŌŁ¼ÓČėČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĒāŃõ»ÆÄĘČÜŅŗ£¬ŹµŃ鏱µĆµ½³ĮµķµÄÖŹĮæÓė¼ÓČėNaOHČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£ŗĒė¼ĘĖćŌŚMµćŹ±ĖłµĆČÜŅŗČÜÖŹÖŹĮæ·ÖŹż£Ø×īŗó½į¹ū¾«Č·µ½0£®1%£©”£
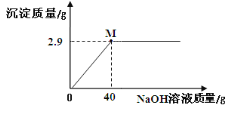
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒė²ĪÓėĻĀĮŠĢ½¾æ»°¶Æ²¢»Ų“šĪŹĢā
£Ø1£©Ģ½¾æ½šŹōµÄŠŌÖŹ£ŗ
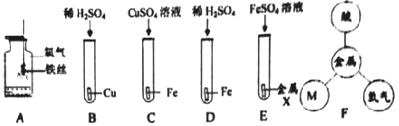
¢ŁĶ¼AÖŠ¼ÆĘųĘæÄŚ·ÅÉŁĮæĖ®µÄÄæµÄ____£¬CÖŠ·“Ó¦µÄĻÖĻóĪŖ____£¬DÖŠµÄ·“Ó¦ ÓŚ__(Ģī»ł±¾·“Ó¦ĄąŠĶ£©
¢ŚĪ§B”śEÖŠÖ»ÓŠB²»·“Ó¦£¬ÓÉŹµņæÉµĆ³öĒāŌŖĖ÷ŗĶČżÖÖ½šŹō»°¶ÆŠŌÓÉ»nÉäīƵÄĖ³ŠņŹĒ_______
¢ŪĶ¼FÖŠµÄMŹō_______(ĢīĪļÖŹĄą±š£©”£
£Ø2£©ČĻŹ¶½šŹōµÄÖʱø£ŗÓĆŅ»Ńõ»ÆĢ¼»¹Ō³ąĢśæó(Ö÷ŅŖ³É·ÖĪŖā»ÆĢś£©µÄ»Æѧ·½³ĢŹ½ĪŖ____.
£Ø3£©»ŲŹÕ·ĻŅŗÖŠ½šŹō£¬Ä³³§ÅųöµÄ·ĻŅŗÖ÷ŅŖŗ¬Zn(NO3)2ŗĶAgNO3,ĪŖĮĖHÄĮ½š¾}AgŗĶZn£ØNO3£©2,ijĶ¬Ń§Éč¼ĘĮĖČēĻĀŹµŃé
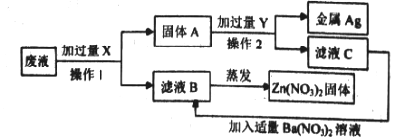
¢Ł²Ł×÷IµÄĆū³ĘŹĒ__________,¼ÓČė¹żĮæXµÄÄæµÄŹĒ__________,
¢ŚĀĖŅŗCµÄÖ÷ŅŖ³É·ÖŹĒ__________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø7·Ö£©½«5%µÄNaOHČÜŅŗÖšµĪ¼ÓČėµ½109Ļ”ŃĪĖįÖŠ£¬±ß¼Ó±ß½Į°č£¬Ėę×ÅNaOHČÜŅŗµÄ¼ÓČė£¬ČÜŅŗpHµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
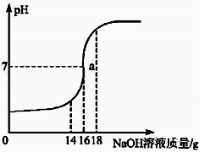
ŹŌ»Ų“š£ŗ
£Ø1£©aµćČÜŅŗÖŠ“óĮæ“ęŌŚµÄĄė×ÓÓŠ ”£
£Ø2£©µ±Ē”ŗĆĶźČ«·“Ó¦Ź±£¬ĻūŗÄNaOHČÜŅŗµÄÖŹĮæĪŖ ”£
£Ø3£©¼ĘĖćĻ”ŃĪĖįÖŠČÜÖŹµÄÖŹĮæ·ÖŹż”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŹµŃéŹŅÅäÖĘ100g 10%µÄĀČ»ÆÄĘČÜŅŗŹ±£¬ŠčŅŖ________gĀČ»ÆÄĘ¹ĢĢ唣³ĘĮæѳʷŹ±£¬Ó¦°Ńѳʷ·ÅŌŚĶŠÅĢĢģĘ½µÄ_________ÅĢĄļ”£
¢Ł³ĘĮæŹ±Čē¹ūÓĆÖŹĮæĪŖ23.1gµÄÉÕ±Ź¢·Å¹ĢĢ壬ŌŚĶŠÅĢĢģĘ½ÉĻŅŃ·Å30gµÄķĄĀė£¬ŌņĢģĘ½ÉĻµÄÓĪĀėĪ»ÖĆÓ¦ŹĒĻĀĶ¼µÄ_____________(Ģī×ÖÄø)”£
¢ŚĻĀĮŠŅĒĘ÷ÖŠ£¬ĮæČ”Ė®Ź±ŠčŅŖÓƵ½dŗĶ____ŅĒĘ÷(ĢīŠņŗÅ)£¬ČܽāŹ±ŠčŅŖÓƵ½eŗĶ____ŅĒĘ÷(ĢīŠņŗÅ)”£(ĆææÕ1·Ö)
a£®ÉÕ±”¢b£®10mLĮæĶ²”¢c£®100mLĮæĶ²”¢d£®µĪ¹Ü”¢e£®²£Į§°ō”¢f£®Ņ©³×”¢g£®Õō·¢Ćó”£
¢ŪĪŖ¼ÓæģŹ³ŃĪµÄČܽāĖŁ¶Č£¬æÉŅŌ²ÉÓƵķ½·ØÓŠ£ŗ_________________Čē¹ūÅäÖʵÄČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹżµĶÓŚ10£„£¬ÄćČĻĪŖæÉÄÜŌŅņŹĒ____________ ”£(ČĪŠ“Ņ»øö)”£
(2)ŌŚ“ÖŃĪĢį“æÖŠ£¬½«ĀČ»ÆÄĘČÜŅŗÕō·¢ÖĮÓŠ½Ļ¶ąĮæ¹ĢĢåĪö³öŗó£¬Ó¦_____£¬_____£¬ĄūÓĆÓąČČ½«ÓąĻĀČÜŅŗÕō·¢ÖĮøÉ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéĢ½¾æŹĒѧĻ°»ÆѧµÄÖŲŅŖ·½·Ø”£
(1)»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§×ćĮæµÄŠæ¼¼¼ÓČėµ½ÅØĮņĖįaÖŠ.·¢ĻÖÓŠ“óĮæµÄĘųÅŻ·Å³ö£¬ĖūĆĒĘųĢåµÄ³É·Ö½ųŠŠĮĖĢ½¾æ”£
”¾Ģį³öĪŹĢā”æŠæĮ£¼ÓČėÅØĮņĖįŗóÉś³ÉµÄĘųĢåŹĒŹ²Ć“£æ
”¾²éŌÄ׏ĮĻ”æ¢ŁÅØĮņĖįÄÜÓėŠæ·“Ó¦£¬µ«²»²śÉśĒāĘų£¬Ņ²²»»į²śÉśŃõĘų£»
¢ŚSO2ÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬Ņ×ČÜÓŚĖ®£¬ÄÜŹ¹Ę·ŗģ£ØŅ»ÖÖŗģÉ«É«ĖŲ£©ČÜŅŗĶŹÉ«”£
”¾Ģį³ö²ĀĻė”æ¼×£ŗĘųĢåŹĒH2£»ŅŅ£ŗĘųĢåŹĒSO2£»±ū£ŗĘųĢåŹĒSO2ŗĶH2£»
”¾ŹµŃéĢ½¾æ”æĪŖĮĖŃéÖ¤ÉĻŹö²ĀĻė”£Ķ¬Ń§ĆĒŌŚĄĻŹ¦µÄÖøµ¼ĻĀÉč¼ĘĮĖČēĻĀĶ¼µÄ×°ÖĆ£Ø²æ·Ö¼Š³ÖĘ÷²ÄĀŌČ„£¬¼ŁÉčĆæøöÄÜ·¢ÉśµÄ·“Ó¦¶¼ĶźČ«½ųŠŠ£©½ųŠŠĢ½¾æ£ŗ
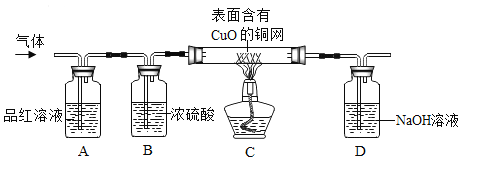
¢ŁŹµŃéæŖŹ¼ŗ󣬹Ū²ģµ½AÖŠĘ·ŗģČÜŅŗĶŹÉ«£¬Ö¤Ć÷ĘųĢåÖŠŗ¬ÓŠ____”£
¢ŚB×°ÖƵÄ×÷ÓĆŹĒ____”£
¢ŪC×°ÖĆŌŚµćČ¼¾Ę¾«µĘ¼ÓČČÖ®Ē°Ó¦ĻČĶØŅ»¶ĪŹ±¼äµÄĘųĢ壬ÄæµÄŹĒ__£»¼ÓČČŅ»¶ĪŹ±¼äŗ󣬹Ū²ģµ½_____£¬Ö¤Ć÷ĘųĢåÖŠŗ¬ÓŠH2”£
”¾ĢÖĀŪ”æ
¢ÜŠæŗĶÅØĮņĖį·“Ӧɜ³ÉĮņĖįŠæ”¢Ė®ŗĶ¶žŃõ»ÆĮņ£¬ĪŖŹ²Ć“ŌŚ·“Ó¦¹ż³ĢÖŠÓÖ²śÉśĮĖĒāĘųÄŲ£æÓĆĪÄ×Ö¼ņŹöŌŅņ£ŗ____”£
¢ŻŠæÓėÅØĮņĖįŗĶĻ”ĮņĖį·“Ó¦¶¼æÉŅŌ²śÉśĮņĖįŠæ£¬Čē¹ūŠčŅŖÖĘČ”ĮņĖįŠæ£¬ÓĆŠæÓėĻ”ĮņĖį·“Ó¦µÄÓŵćŹĒ____£ØČĪĢīŅ»ÖÖŗĻĄķµÄ“š°ø£©”£
(2)Ģ¼ĖįĒāÄĘ£ØNaHCO3£©Ė×³Ę”°Š”ĖÕ“ņ”±£¬ŌŚÉś»īÖŠÓĆĶ¾¹ć·ŗ£®Ä³»ÆѧŹµŃ銔×éµÄĶ¬Ń§¶ŌĢ¼ĖįĒāÄʵĊŌÖŹ½ųŠŠĢ½¾æ£®
”¾Ģ½¾æŹµŃé1”æĢ¼ĖįĒāÄĘČÜŅŗµÄĖį¼īŠŌ
ÓĆŹŌ¹ÜČ”ŹŹĮæĢ¼ĖįĒāÄĘČÜŅŗ£¬µĪ¼Ó·ÓĢŖŹŌŅŗ£¬Õńµ“£¬ČÜŅŗ±äĒ³ŗģÉ«£®½įĀŪ£ŗ____£®
”¾Ģ½¾æŹµŃé2”æÄÜÓėĖį·“Ó¦
Č”ŹŹĮæĢ¼ĖįĒāÄĘ¼ÓČėŹŌ¹ÜÖŠ£¬µĪ¼ÓĻ”ŃĪĖį£¬ŌŁ°ŃČ¼×ŵÄľĢõŃøĖŁÉģČėŹŌ¹Ü£¬Ä¾ĢõĻØĆš£¬Ģ¼ĖįĒāÄĘŗĶŃĪĖįµÄ»Æѧ·“Ó¦·½³ĢŹ½£ŗ____£®
”¾Ģ½¾æŹµŃé3”æÄÜÓė¼ī·“Ó¦
²éŌÄ׏ĮĻ£ŗNaHCO3+NaOHØTNa2CO3+H2O£»ĒāŃõ»ÆøĘĪ¢ČÜÓŚĖ®£®ÓĆŹŌ¹ÜČ”ŹŹĮæĢ¼ĖįĒāÄĘČÜŅŗ£¬µĪ¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬ĪŽĆ÷ĻŌĻÖĻ󣮣ØĢįŹ¾£ŗæÉŅŌŃ”ŌńCaCl2ČÜŅŗ×öŹŌ¼Į£¬ĶعżÖ¤Ć÷ÓŠNa2CO3Éś³É£¬“Ó¶ųÖ¤Ć÷¶žÕß·¢ÉśĮĖ·“Ó¦£©ČēĶ¼£¬Į½Ī»Ķ¬Ń§·Ö±š½ųŠŠĮĖ¼×”¢ŅŅĮ½øöŹµŃ飮»Ų“šĻĀĮŠĪŹĢā£ŗ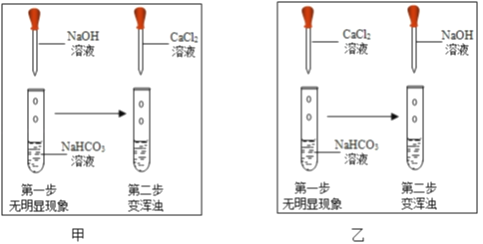
±Č½Ļ¼×”¢ŅŅĮ½øöŹµŃéµÄÄæµÄŠŌĒų±šŹĒ____£»
ÓŠĶ¬Ń§Ģį³öĮ½øöŹµŃ鶼²»×ćŅŌÖ¤Ć÷ÓŠNa2CO3Éś³É£¬ĘäĄķÓÉŹĒ____£»ŅŖÖ¤Ć÷ÓŠNa2CO3Éś³É£¬»¹ŠčŅŖ½ųŠŠµÄ²Ł×÷ŹĒ____£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¼Ź¾ÖŠA”Ŗ”ŖFŹĒ³õÖŠ»Æѧ³£¼ūµÄĪļÖŹ”£°“µ„ÖŹ”¢Ńõ»ÆĪļ”¢Ėį”¢¼ī”¢ŃĪ·ÖĄą£¬A”¢B”¢C”¢D”¢EŹĒĪåÖÖ²»Ķ¬Ąą±šµÄĪļÖŹ£¬FŹĒ“óĄķŹÆµÄÖ÷ŅŖ³É·Ö”£Ķ¼ÖŠ”°--”±±ķŹ¾ĻąĮ¬µÄĮ½ÖÖĪļÖŹÖ®¼äæÉŅŌ·¢Éś·“Ó¦£¬”°”ś”±±ķŹ¾ĪļÖŹ¼ä“ęŌŚ×ÅĻąÓ¦µÄ×Ŗ»Æ¹ŲĻµ(²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļ¼°·“Ó¦Ģõ¼žŅŃĀŌČ„)”£Ēė»Ų“š£ŗ
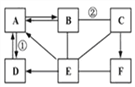
(1)ĪļÖŹFµÄ»ÆѧŹ½__________£»
(2)·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½____________________£»
(3)·“Ó¦¢ŁµÄ»ł±¾·“Ó¦ĄąŠĶŹĒ_____________£»
(4)EŹĒÓÉĮ½ÖÖŌŖĖŲ×é³ÉµÄ£¬ĒėŠ“³öĘäµÄŅ»ÖÖÓĆĶ¾_______”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com