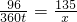解:(1)根据反应的式子可以看出,反应后有1个铜原子,2个钠原子,两个氯原子,1个硫原子和4个氧原子,故氯化钠前面的数字为2,氧气前面的数字为2,故填:2,2;
(2)测定溶液的pH时,可以用玻璃棒蘸取待测液涂在pH试纸上,把显示的颜色与标准比色卡对照,即可得出溶液的pH,故填:用玻璃棒蘸取待测液涂在pH试纸上,把显示的颜色与标准比色卡对照,即可得出溶液的pH;
(3)硫化铜焙烧后可能生成二氧化硫,二氧化硫是空气污染物,直接排放到空气中会污染空气,故答案为:不能,焙烧后的尾气中含有二氧化硫,会污染空气;
(4)废渣中硫元素的质量分数为24%,则硫元素的质量为:500t×24%=120t
硫化铜的质量为:120t÷
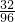
=360t
设生产出氯化铜的质量为x
CuS+2NaCl+2O
2═CuCl
2+Na
2SO
4
96 135
360t x
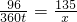
x=506.3t
答:理论可以生产出506.3吨氯化铜.
分析:根据已有的知识进行分析,化学反应前后原子的种类和原子的个数不变,据此可以得出化学式前面的计量数,根据测定溶液pH的方法进行解答,焙烧后的气体中含有二氧化硫,不能直接排放到空气中,根据反应的化学方程式即可计算得出生成氯化铜的质量.
点评:本题考查了物质制备的有关知识,完成此题,可以依据物质的性质进行.

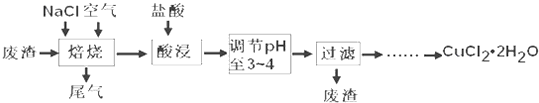
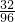 =360t
=360t