


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
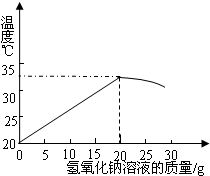 某化学兴趣小组的同学要配制200g质量分数为20%的氢氧化钠溶液.下图表示用配出的溶质质量分数为20%氢氧化钠溶液与20g某稀盐酸发生反应后溶液温度的变化情况.
某化学兴趣小组的同学要配制200g质量分数为20%的氢氧化钠溶液.下图表示用配出的溶质质量分数为20%氢氧化钠溶液与20g某稀盐酸发生反应后溶液温度的变化情况.查看答案和解析>>
科目:初中化学 来源:2010年九年级化学测试试卷(2)(解析版) 题型:填空题
查看答案和解析>>
科目:初中化学 来源:专项题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com