
 ��ͼ�Ƿѿ���������ʤ�ڡ����ۡ����ŷɴ��е���Ƭ������ӻ�ѧ���ӽǶ������ɴ����й���Ϣ����˼��������
��ͼ�Ƿѿ���������ʤ�ڡ����ۡ����ŷɴ��е���Ƭ������ӻ�ѧ���ӽǶ������ɴ����й���Ϣ����˼������������ ��1�����ݴ���������һ��������ɵ����ʽ��з�����
��2�����ݺ���Ա���ĵ������������������ܶȽ��м��㣻
��3�����ݿ����ijɷֽ��м��㣮
��� �⣺��1������������һ��������ɵ����ʣ��������ڴ��������������ˮ��������̼��
��2����λ����Ա��̫����ÿ���Լ��Ҫ�������������$\frac{2��0.9kg��1000}{1.43g/L}$=1258.7L��
��3��ʹ�ò�������ɷִ��º͵��汣��һ�µķ����ǣ��ٻ���ʱ���Ƶ����������������ԼΪ4��1���ڲ��ϲ������������ռ������Ķ�����̼�����ռ��ų���ˮ������
�ʴ�Ϊ����1��������ˮ��������̼��
��2��1258.7L��
��3���ٻ���ʱ���Ƶ����������������ԼΪ4��1���ڲ��ϲ������������ռ������Ķ�����̼�����ռ��ų���ˮ������
���� ������Ҫ����Ŀ����ɷֵ����֪ʶ���ѶȲ�����Ҫ��ƽʱ��ǿ���伴����ɣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ձ���ú��ȼ�� | B�� | �ƹ�ֲ������ | ||
| C�� | �ᳫʹ�������� | D�� | �ƹ�ʹ������ϴ�·� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{9}{12}$ | B�� | $\frac{12}{9}$ | C�� | $\frac{33}{32}$ | D�� | $\frac{32}{33}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���µĿ��� | B�� | ��Ȫˮ | C�� | ��ˮ������ | D�� | �����ʯ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
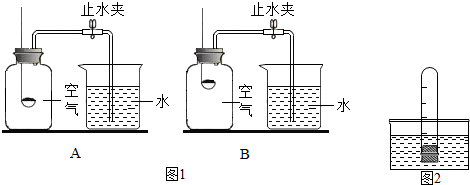
| �� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| ����ƿ�ڽ���ˮ�������mL�� | 40 | 35 | 40 | 40 | 40 | 45 | 40 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �� | ������ | �������� |
| ���� | ˮ�� | ��ʯ�� | ��ʯ�һ���ʯ�� |
| ��ѧʽ | Hg | CaO | Ca��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 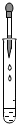 �μ�Һ�� | B�� | 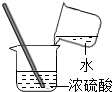 ϡ��Ũ���� | C�� | 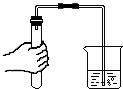 ��������� | D�� |  Ϩ��ƾ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com