
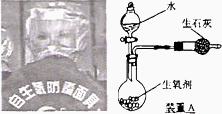
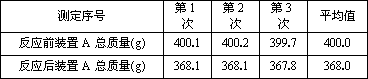
下图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2某研究小组取100 g生氧剂,放人装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量,他们进行了三次实验.测定结果如下:
请根据上述实验结果计算:(假设杂质不与水反应产生气体)
(1)100 g生氧剂与足量水反应生成的氧气质量;
(2)生氧剂中KO2的质量分数;
(3)若成人每分钟正常需氧量为0.32 g,则能维持成人正常呼吸20分钟的“化学氧自救器”,至少要装入这种生氧剂多少克?(注:第(3)小题不必写出解题过程)
科目:初中化学 来源: 题型:058
(2007
,福建省厦门市,25)下图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是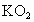 )的作用原理为:
)的作用原理为: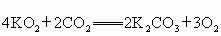
某研究小组取
100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为: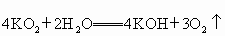 ),测定反应前后装置A的总质量,他们进行了三次实验.
),测定反应前后装置A的总质量,他们进行了三次实验.

测定结果如下:

请根据上述实验结果计算:
(假设杂质不与水反应产生气体)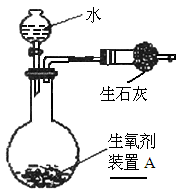
(1)100g
生氧剂与水反应生成的氧气质量;(2)
生氧剂中含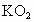 的质量分数;
的质量分数;
(3)
若成人每分钟正常需氧量约为0.32g,则能维持成人正常呼吸20分钟的“化学氧自救器”,至少要装入这种生氧剂多少克?(注:第(3)小题不必写出解题过程)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com