
 ”“
”“ ”“
”“ ”分别代表不同元素的原子)
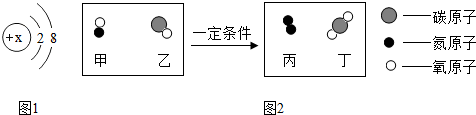
”分别代表不同元素的原子)分析 (1)根据保持水的化学性质的最小粒子是水分子进行解答;
(2)根据带负电荷是得到电子,带正电荷是失去电子进行解答;
(3)根据单质的定义和化学反应的实质进行解答;根据图中所示,可写出反应的化学方程式,进而求出丙和丁的质量比;
解答 解:(1)保持水的化学性质的最小粒子是水分子,其化学式为:H2O;
(2)粒子R-是R原子得到1个电子得到的,由粒子R-的结构示意图,则x=2+8-1=9.
(3)①单质是由一种元素组成的纯净物,故属于单质的为丙;
②在化学反应前面原子的质量、个数和种类不变,故元素的种类和质量也不会变,故选AC;
③由图可知,该反应的化学方程式为:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;故丙和丁的质量比为(14×2):(12×2+16×4)=7:22
故答案为:(1)H2O (2)9 (3)①丙 ②AC ③7:22
点评 本题考查较为全面,要正确解答本题,依据已有知识即可.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 钼是稀有的矿产资源,主要用于航天合金材料制作.在元素周期表中钼元素的某些信息如图所示,下列有关钼的说法正确的是( )
钼是稀有的矿产资源,主要用于航天合金材料制作.在元素周期表中钼元素的某些信息如图所示,下列有关钼的说法正确的是( )| A. | 相对原子质量为95.94g | B. | 原子核内质子数为42 | ||
| C. | 属于非金属元素 | D. | 元素符号为MO |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验一 | 实验二 | 实验三 |
观察固体表面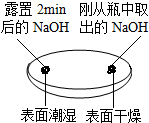 | 向两块固体表面滴加稀盐酸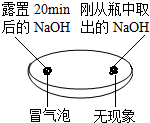 | 振荡三个塑料瓶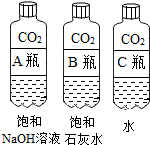 |
| 方案一 | 方案二 | 分析 |
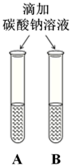 | 微热(不考虑水分蒸发)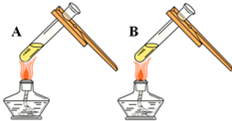 | 两种方案中均观察到A试管内出现白色浑浊,A中试剂为氢氧化钠溶液; 方案二的A溶液变浑浊的原因是氢氧化钙的溶解度随温度升高而减少;氢氧化钠的溶解度随温度升高而升高;两者的溶解度受温度影响情况不同. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
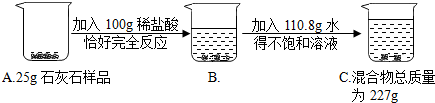
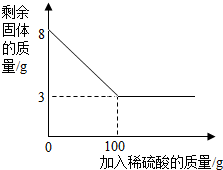 小朋同学为测定某种混合物(成分Fe2O3和C)中Fe2O3的含量,称取8g样品与稀硫酸反应,得到数据如图所示.请回答下列问题:
小朋同学为测定某种混合物(成分Fe2O3和C)中Fe2O3的含量,称取8g样品与稀硫酸反应,得到数据如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com