
水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)净水器中常用到活性炭,其作用是__________________。
(2)水常用来配制各种溶液,氯化铁溶液中的溶质为___________(写化学式)。
(3)农业生产常用溶质的质量分数为10% ~ 20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,稀释后溶液的质量为________g。
(4)根据下表回答问题。
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度 /g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
77.3 |
①40 ℃时,向两个分别盛有40 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为不饱和溶液的是____________溶液。
②采用一种操作方法,将上述的不饱和溶液变为饱和溶液。下列说法正确的是________(填字母序号)。
A.溶质的质量一定不变 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可升高温度或减少溶剂
(1)吸附 (2)FeCl3 (3)500g (4)①NH4Cl ② C
【解析】
试题分析:(1)由于活性炭具有疏松多孔的结构,故具有较强的吸附性,能吸附色素和异味。
(2)根据溶质和溶剂的相互关系,以及溶液的命名方法可知,氯化铁溶液即为氯化铁的水溶液,故其中的溶质为氯化铁,由于氯化铁中铁元素的化合价为+3,氯元素的化合价为-1,故氯化铁的化学式为FeCl3。
(3)将300g25%的NaCl溶液稀释为15%的NaCl溶液,需要加水,故在溶液稀释的过程中,改变的是溶剂的质量,不变的是溶质的质量,据此列式计算;设稀释后的溶液的质量为x,则有300g×25%=15%x,解得x=500g。
(4)①根据溶解度表中的数据可知,在40℃时,氯化钠的溶解度为36.6g,氯化铵的溶解度为45.8g,即在40℃时,每100g水中,最多溶解氯化钠36.6g,氯化铵45.8g而达到饱和状态;故在此温度下,向两个分别盛有40g NaCl和NH4Cl的烧杯中,各加入100g的水,充分溶解后,得到的是NaCl的饱和溶液和NH4Cl的不饱和溶液。
②要将某不饱和溶液变为饱和溶液,最常用的方法是加入溶质,故溶质质量可能改变;根据溶解度表中的数据可知,NaCl和NH4Cl的溶解度都随温度的升高而增大,故要将其不饱和溶液变为饱和溶液,可用降温的方法,而在降低温度的过程中,溶质、溶剂的质量均不变,则溶液的质量可能不变,溶质质量分数也可能不变,故选C。
考点:碳单质的物理性质及用途,溶液、溶质和溶剂的相互关系与判断,用水稀释改变浓度的方法,饱和溶液和不饱和溶液,饱和溶液和不饱和溶液相互转变的方法,固体溶解度的影响因素
点评:本题主要考查的是有关溶液的知识,涉及到的知识点较多,难度适中,只要学生熟练掌握相关基础知识,即可正确做出解答。


科目:初中化学 来源: 题型:
 (2013?通州区一模)水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与溶解度曲线(图1),回答下列问题:
(2013?通州区一模)水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与溶解度曲线(图1),回答下列问题:| 温度/°C 溶解度/g |
0 | 20 | 40 | 60 | 80 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?昌平区二模)水和溶液在生命活动和生产、生活中起着十分重要的作用.
(2012?昌平区二模)水和溶液在生命活动和生产、生活中起着十分重要的作用.
| ||
| ||
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
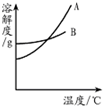 水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与
水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与| 温度/℃ 溶解度/g |
0 | 20 | 40 | 60 | 80 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
查看答案和解析>>
科目:初中化学 来源:2012届北京市昌平区中考二模化学试卷 题型:填空题
(6分)水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)净水器中经常使用活性炭,主要利用活性炭的_______性。
(2)根据图中实验只生成了氢气和氧气,确定水是由氢元素和氧元素组成的,得到此结论的依据是________。写出此实验中发生反应的化学方程式________。
(3)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com