
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:要除去KN03溶液中的KCl,实质就是除去氯离子,可利用氯化钾溶液与硝酸银溶液反应生成氯化银沉淀和硝酸钾溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:KCl+AgNO3═KNO3+AgCl↓.
要除去NaCl溶液中的Na2CO3,实质就是除去碳酸根离子,可利用碳酸钠溶液与适量的稀盐酸反应生成氯化钠、水和二氧化碳,至不再产生气泡为止,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑(合理即可).
要除去NaNO3溶液中的CuS04,实质就是除去铜离子和硫酸根离子,可利用CuS04溶液与适量的氢氧化钡反应生成硫酸钡沉淀和氢氧化铜沉淀,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Ba(OH)2+CuSO4=Cu(OH)2↓+BaSO4↓.
要除去NaCl溶液中的MgCl2,实质就是除去镁离子,可利用MgCl2溶液与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl.
要除去FeS04溶液中的CuSO4,实质就是除去铜离子,可利用CuSO4溶液与足量的铁粉反应生成硫酸亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故答案为:KCl+AgNO3═KNO3+AgCl↓;Na2CO3+2HCl═2NaCl+H2O+CO2↑(合理即可);Ba(OH)2+CuSO4=Cu(OH)2↓+BaSO4↓;2NaOH+MgCl2═Mg(OH)2↓+2NaCl;Fe+CuSO4═FeSO4+Cu.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 使用现象 | 对比结论 |
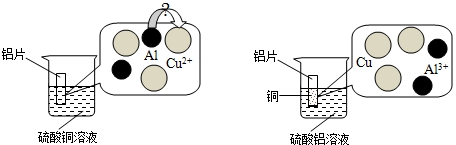
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出. | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体. | 现象一与现象二对比,说明 ①A |
| 现象二:粗砂纸打磨的片刻内现象不明显. | ||
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出. | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体. | 现象三与现象一对比,说明 ②B |
| 现象四:特细砂纸打磨的表面一段时间内没有明显现象. | 现象四与现象三对比,说明 ③C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com