
| A. | 烧制陶瓷 | B. | 发明指南针 | C. | 使用火药 | D. | 冶炼钢铁 |
分析 根据化学的定义和研究内容进行分析判断,化学是一门研究物质的组成、结构、性质及其变化规律的科学,研究对象是物质,研究内容有组成、结构、性质、变化、用途等;属于化学成就的,在变化过程中都有其他物质生成
解答 解:A、烧制陶瓷,属于研究、制取的新物质,属于我国古代化学工艺成就,故选项错误.
B、指南针的发明只涉及到物理变化,不属于化学工艺,不属于我国古代化学工艺成就,故选项正确.
C、使用火药,利用了硝石、硫、碳发生化学反应生成二氧化硫、二氧化碳、氮气、硫酸钾等产物,属于我国古代化学工艺成就,故选项错误.
D、冶炼钢铁,属于研究、制取的新物质,属于我国古代化学工艺成就,故选项错误.
故选B.
点评 了解化学研究的内容,才能利用化学知识服务于社会,造福于人类,有利于培养学生的学习兴趣,提高社会责任感.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
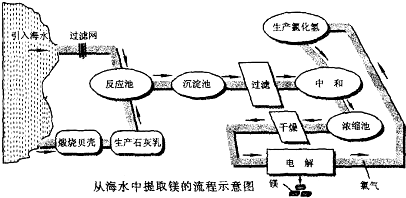
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
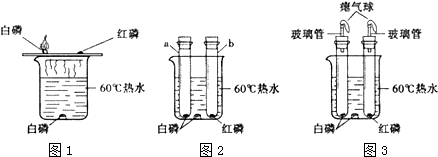
| 现象 | 解释 |
| a试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. | b试管中红磷、热水中白磷都没有燃烧的原因是①温度未达到红磷的着火点;②热水中的白磷没有与氧气(空气)接触. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钡(硫酸钾) | B. | 氢氧化钠(稀硫酸) | C. | 稀硫酸(氯化钡) | D. | 稀盐酸(碳酸钠) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
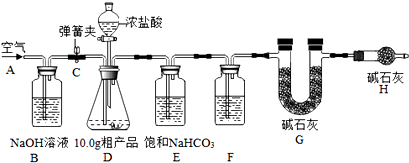
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有发光发热的一定是燃烧 | |
| B. | 燃烧一定有火焰 | |
| C. | 燃烧一定有化学变化 | |
| D. | 要使火熄灭,必须使可燃物隔绝空气,而且使温度降到着火点以下 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
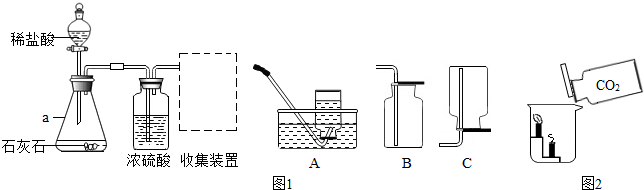
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com