
分析 ①原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
②分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字.
③离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
④化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后.
⑤标在元素符号右上角的数字表示1个离子所带的电荷数.
⑥地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝.
解答 解:①由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氢原子表示为:2H.
②由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则二氧化氮分子可表示为:NO2.
③由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.氢氧根离子可表示为:OH-.
④五氧化二磷中氧元素显-2价,磷元素的化合价是+5价;由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故五氧化二磷中磷元素的化合价为+5价可表示为:$\stackrel{+5}{P}$2O5.
⑤标在元素符号右上角的数字表示1个离子所带的电荷数,Fe2+中的“2”表示一个亚铁离子带有两个单位的正电荷.
⑥地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝,氧化铝中铝元素显+3价,氧元素显-2价,其化学式为:Al2O3.
故答案为:①2H;②NO2;③OH-;④$\stackrel{+5}{P}$2O5;⑤一个亚铁离子带有两个单位的正电荷;⑥Al2O3.
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、化学式、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 事实 | 解释 |
| A | 一氧化碳和二氧化碳化学性质不同 | 分子构成不同 |
| B | 通过气味辨别白酒和白醋 | 分子在不断的运动,不同分子的性质不同 |
| C | 密封良好的方便面从平原带到高原时,包装袋鼓起 | 分子体积增大 |
| D | 食物腐败 | 生成了新的分子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
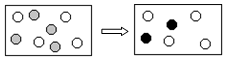 一瓶NaOH溶液在空气中完全变质,图中小球分别表示在变质前后溶液中存在的主要离子,其中“●”表示的微粒是( )
一瓶NaOH溶液在空气中完全变质,图中小球分别表示在变质前后溶液中存在的主要离子,其中“●”表示的微粒是( )| A. | Na+ | B. | OH- | C. | CO32- | D. | H+ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com