
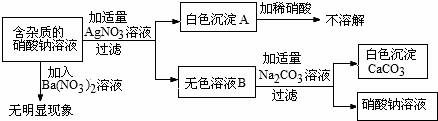
分析 根据题意可知,向含杂质的硝酸钠溶液加入硝酸钡溶液不产生沉淀,说明了溶液中不含有碳酸根离子和硫酸根离子;加入适量的硝酸银溶液产生了不溶于稀硝酸的白色沉淀,说明了溶液中含有氯离子;向过滤后的滤液中加入适量的碳酸钠溶液产生了碳酸钙沉淀,说明了溶液中含有钙离子,由此可知溶液含有的杂质是氯化钙,据此分析回答由管的问题.
解答 解:由题意可知,向含杂质的硝酸钠溶液加入硝酸钡溶液不产生沉淀,说明了溶液中不含有碳酸根离子和硫酸根离子;加入适量的硝酸银溶液产生了不溶于稀硝酸的白色沉淀,说明了溶液中含有氯离子;向过滤后的滤液中加入适量的碳酸钠溶液产生了碳酸钙沉淀,说明了溶液中含有钙离子,由此可知溶液含有的杂质是氯化钙.
(1)由上述分析可知,白色沉淀A为氯化银,化学式为:AgCl;
(2)由于硝酸银与氯化钙反应生成了氯化银白色沉淀和硝酸钙,所以,过滤后的无色溶液B中含有的溶质有硝酸钠、硝酸钙;加入碳酸钠溶液后碳酸钠与硝酸钙反应生成了碳酸钙沉淀和硝酸钠,发生反应的化学方程式是:Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3;
(3)由上述分析可知,含杂质的硝酸钠溶液中含有氯化钙,所以“含杂质的硝酸钠溶液”中含有的离子有:Ca2+、NO3-、Na+、CO32-.
故答为:(1)AgCl;(2)硝酸钠、硝酸钙,Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3;(3)Ca2+、NO3-、Na+、CO32-.
点评 本题主要考查了混合物中含有杂质的确定,解答本题的关键是掌握常见离子检验方法.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:填空题
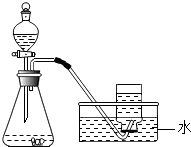 下列制取和收集气体的方案,可以直接采用如图所示装置进行的是CD
下列制取和收集气体的方案,可以直接采用如图所示装置进行的是CD查看答案和解析>>
科目:初中化学 来源: 题型:解答题
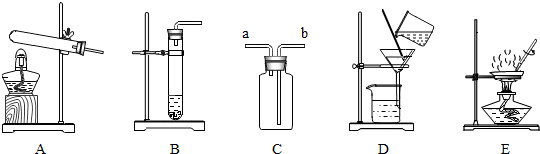
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
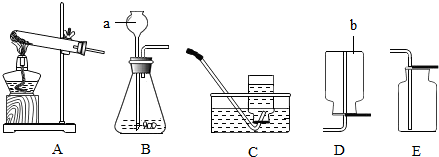
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
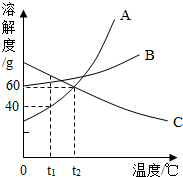 如图是A、B、C三种物质的溶解度曲线,回答下列问题:
如图是A、B、C三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 焚烧秸秆增加肥力 | B. | 城区严禁燃放烟花爆竹 | ||
| C. | 大力发展电力公交 | D. | 关闭燃煤小锅炉 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
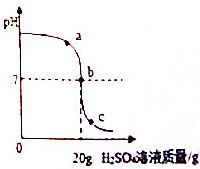 化学小组探究酸碱中和反应时,利用溶质质量分数为4.9%的稀硫酸来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示.
化学小组探究酸碱中和反应时,利用溶质质量分数为4.9%的稀硫酸来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 感官指标 | 化学指标 | 细菌指标 |
| 水质无色无味澄清 | pH6.5-8.5 | 细菌总数<100个/ml等 |
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com