
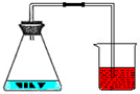
 øł¾ŻČēĶ¼ĖłŹ¾µÄ”°ĢśÉśŠāŹµŃé”±£¬»Ų“šĻĀĮŠĪŹĢā£®Č”Ņ»æé·Ļ¾ÉµÄĢśĖ棬½«Ęä¼ō³É¼øŠ”ʬ£¬ÓĆĻ”ŃĪĖį½žÅŻĘ¬æĢ£®·ÅČė׶ŠĪĘæÖŠ£¬ŌŁĻņ׶ŠĪĘæÖŠ¼ÓČė3mL-4mLÅØŹ³ŃĪĖ®ČóŹŖĢśĖ棬Čū½ō“ųµ¼¹ÜµÄµ„æ×Čū£¬µ¼¹ÜµÄĮķŅ»¶ĖČūČėŗģÉ«µÄĖ®ÖŠ£¬¼ø·ÖÖÓŗ󣬹Ū²ģĻÖĻó£®
øł¾ŻČēĶ¼ĖłŹ¾µÄ”°ĢśÉśŠāŹµŃé”±£¬»Ų“šĻĀĮŠĪŹĢā£®Č”Ņ»æé·Ļ¾ÉµÄĢśĖ棬½«Ęä¼ō³É¼øŠ”ʬ£¬ÓĆĻ”ŃĪĖį½žÅŻĘ¬æĢ£®·ÅČė׶ŠĪĘæÖŠ£¬ŌŁĻņ׶ŠĪĘæÖŠ¼ÓČė3mL-4mLÅØŹ³ŃĪĖ®ČóŹŖĢśĖ棬Čū½ō“ųµ¼¹ÜµÄµ„æ×Čū£¬µ¼¹ÜµÄĮķŅ»¶ĖČūČėŗģÉ«µÄĖ®ÖŠ£¬¼ø·ÖÖÓŗ󣬹Ū²ģĻÖĻó£®·ÖĪö øł¾ŻĢśÉśŠāµÄÖŖŹ¶½ųŠŠ·ÖĪö£¬ĢśŌŚÓŠĖ®ŗĶŃõĘų²¢“ꏱŅ×ÉśŠā£¬¾Ż“Ė½ā“š£¬ŌŚĖįÄÜÓėĢśŠā·“Ó¦£¬ŃĪÄÜŹ¹“Ł½ųĢśµÄŠāŹ“£®
½ā“š ½ā£ŗĢśĖæ±»Ź³ŃĪĖ®½žŹŖ£¬ÓėŃõĘųŗĶĖ®Ķ¬Ź±½Ó“„£¬ŌņĢśČŻŅ×ÉśŠā£¬ĢśÉśŠāĻūŗÄŃõĘų£¬µ¼ÖĀ׶ŠĪĘæÄŚµÄŃ¹Ēæ±äŠ”£¬ÉÕ±ÖŠµÄŗģÄ«Ė®ŌŚ“óĘųŃ¹µÄ×÷ÓĆĻĀŃŲµ¼¹ÜÉĻÉżŠĪ³ÉŅ»¶ĪŅŗÖł£¬ĢśŠāµÄÖ÷ŅŖ³É·ÖŹĒŃõ»ÆĢśÓėĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆĢśŗĶĖ®£¬½«ĢśŠā³żČ„£»ÅØŹ³ŃĪĖ®¼ÓæģĮĖĢśµÄŠāŹ“£®
¹ŹĢī£ŗĢś£ØĖ棩ӊŅų°×É«±äĪŖŗģ×ŲÉ«£»²åČėÉÕ±ÖŠµÄµ¼¹ÜÄŚÓŠŗģÉ«Ė®ÖłÉĻÉżŅ»Š”¶Ī£®ĢśŌŚ³±ŹŖµÄæÕĘųÖŠŅ×ÉśŠā£»ĶæÓĶ»ņÅēĘį»ņ±£³Ö±ķĆęøÉŌļ£»³żĢśŠā£»Ģį¹©Ė®·Ö£»¼ÓæģĢśÉśŠā£®
µćĘĄ ±¾Ģāæ¼²éĮĖĢśÉśŠāµÄĢõ¼ž£¬Ķź³É“ĖĢā£¬æÉŅŌŅĄ¾ŻŅŃÓŠĢśÉśŠāµÄÖŖŹ¶½ųŠŠ£®


 ŠĒ¼¶æŚĖćĢģĢģĮ·ĻµĮŠ“š°ø
ŠĒ¼¶æŚĖćĢģĢģĮ·ĻµĮŠ“š°ø Ć¢¹ū½ĢøØ“ļ±ź²āŹŌ¾ķĻµĮŠ“š°ø
Ć¢¹ū½ĢøØ“ļ±ź²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
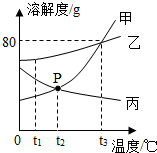 Ķ¼¼×”¢ŅŅ”¢±ūČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻߣ¬Ēė»Ų“šĻĀĮŠĪŹĢā£®
Ķ¼¼×”¢ŅŅ”¢±ūČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻߣ¬Ēė»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö±½ÓŌŚĘææŚĪÅŅ©Ę·µÄĘųĪ¶ | B£® | ÓĆŅ©³×Č”ÓĆ·ŪĩדŅ©Ę· | ||
| C£® | ÓĆ×ģ“µĆš¾Ę¾«µĘ | D£® | Č”ĻĀŹŌ¼ĮĘæČū£¬Õż·ÅŌŚ×ĄÉĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗµÄÅØ¶Č | B£® | ČÜŅŗµÄÖŹĮæ | C£® | ČÜÖŹµÄÖŹĮæ | D£® | ČܼĮµÄÖŹĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
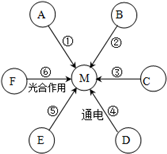 A”¢B”¢D¾łĪŖ“æ¾»Īļ£¬C”¢E”¢F¾łĪŖ»ģŗĻĪļ£»¢Ł”«¢ŽĮłĢõĶ¾¾¶£ØČēĶ¼£©¶¼»į²śÉśĘųĢåM£¬ŹµŃéŹŅæÉĄūÓĆĶ¾¾¶¢Ł”¢¢Ś”¢¢Ū·“Ó¦Ą“ÖĘČ”M£¬Ķ¾¾¶¢Ł”¢¢Ś”¢¢Ū”¢¢Ü·“Ó¦ĄąŠĶĻąĶ¬£¬Ķ¾¾¶¢Ł·“Ӧɜ³ÉµÄŅ»ÖÖĪļÖŹNæÉ×÷ĪŖĶ¾¾¶¢Ś”¢¢Ū·“Ó¦µÄ“߻ƼĮ£®
A”¢B”¢D¾łĪŖ“æ¾»Īļ£¬C”¢E”¢F¾łĪŖ»ģŗĻĪļ£»¢Ł”«¢ŽĮłĢõĶ¾¾¶£ØČēĶ¼£©¶¼»į²śÉśĘųĢåM£¬ŹµŃéŹŅæÉĄūÓĆĶ¾¾¶¢Ł”¢¢Ś”¢¢Ū·“Ó¦Ą“ÖĘČ”M£¬Ķ¾¾¶¢Ł”¢¢Ś”¢¢Ū”¢¢Ü·“Ó¦ĄąŠĶĻąĶ¬£¬Ķ¾¾¶¢Ł·“Ӧɜ³ÉµÄŅ»ÖÖĪļÖŹNæÉ×÷ĪŖĶ¾¾¶¢Ś”¢¢Ū·“Ó¦µÄ“߻ƼĮ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com