

| A. | 该反应为化合反应 | B. | 丙一定没有参加反应 | ||
| C. | 反应中甲、乙改变的质量比为1:3 | D. | 丁相对分子质量是甲的2倍 |
分析 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.反应后质量增加的是生成物,减少的是反应物,据此分析.
解答 解:根据质量守恒定律,反应后丁的质量为:4g+10g+3g+4g-(6g+4g+3g)=8g,故乙为反应物,甲、丁为生成物,丙可能为催化剂,该反应为分解反应,
A、该反应为分解反应,故错误;
B、丙的质量没变可能没有参加反应,也可能为催化剂,故不正确;
C、生成甲、乙的质量比为:(6g-4g):(10g-4g)=1:3,故正确;
D、生成甲、丁的质量比为:(6g-4g):(8g-4g)=1:2,由于未知反应的化学方程式中的化学计量数,故无法确定甲、丁的相对分子质量比,故选项说法错误;
故选C.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.


科目:初中化学 来源: 题型:多选题
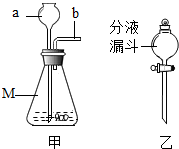 如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )| A. | M所指仪器的名称是广口瓶 | |
| B. | 仪器a、b插入双孔橡皮塞的先后顺序是先a后b | |
| C. | 甲装置也可以用作实验室制氧气和氢气的发生装置 | |
| D. | 将甲中a换成仪器乙,优点是能控制反应的发生与停止 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
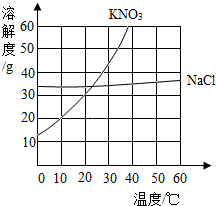 根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸的用量 | 5g | 5g | 5g | 5g |
| 剩余固体的质量 | 3g | 2g | 1g | 1g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量白色固体加入足量CaCl2 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 过滤、取少量滤液加入无色酚酞试液 | 试液变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 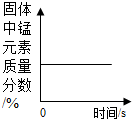 加热一定量的高锰酸钾固体 | |
| B. | 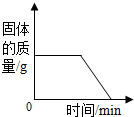 木炭在高温下和氧化铜反应 | |
| C. | 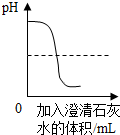 向一定量的盐酸中加澄清石灰水 | |
| D. | 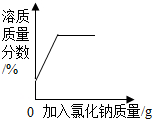 20℃时,向一定量接近饱和的氯化钠溶液中加入氯化钠固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
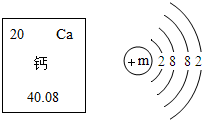 如图是钙元素在元素周期表中的信息和该原子的原子结构示意图,据此判断,下列说法正确的是( )
如图是钙元素在元素周期表中的信息和该原子的原子结构示意图,据此判断,下列说法正确的是( )| A. | 钙原子的相对原子质量为40.08g | |
| B. | 钙原子的结构示意图中m为20 | |
| C. | 钙属于非金属元素 | |
| D. | 在化学反应中,钙原子容易得到2个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com