
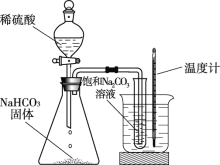
【题目】向饱和碳酸钠溶液中通入CO2会析出碳酸氢钠晶体而是溶液变浑浊,发生反应的化学方程式为Na2CO3 + CO2 + H2O = 2NaHCO3。某化学小组同学用下图装置探究影响碳酸氢钠晶体产生快慢的因素,结果如下表。下列判断不正确的是
序号 | 温度/℃ | CO流速 (个气泡/秒) | 出现浑浊 的时间 |
① | 25 | 5~8 | 5′17″ |
② | 40 | 5~8 | 3′48″ |
③ | 25 | 10~13 | 5′02″ |
④ | 25 | 2~5 | 5′40″ |
A. 锥形瓶中反应的化学方程式为2NaHCO3 + H2SO4 = Na2SO4 + H2O + CO2↑
B. ①②对比可知,其他条件相同时,温度越高,析出晶体越快
C. ③④对比可知,其他条件相同时,CO2流速越大,析出晶体越快
D. ①③对比可知,二氧化碳的流速是影响析出晶体快慢的主要因素
【答案】D
【解析】
A. 由反应装置图可知,锥形瓶中碳酸氢钠与稀硫酸反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:2NaHCO3 + H2SO4 = Na2SO4 + H2O + CO2↑,说法正确;故不符合题意;
B. 由①②对比可知,其他条件相同时,温度越高,析出晶体所需时间越短,析出晶体越快,说法正确,故不符合题意;
C. 由③④对比可知,其他条件相同时,CO2流速越大,析出晶体所需的时间越短,故析出晶体越快,说法正确,故不符合题意;
D. 由①③对比可知,二氧化碳的流速对于析出晶体快慢影响不大,不是主要因素,通过对比①②可以看出温度才是影响析出晶体的主要因素。说法错误,故符合题意;
故选D


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线交于点P.据图回答:
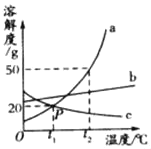
(1)P点的含义是_____。
(2)t1℃时,30g的a物质加入到50g水中不断搅拌,能形成80g溶液吗?_____(填“能”或“不能”)
(3)t2℃时a、b、c三种物质的溶解度由大到小的顺序排列的是_____(填写物质序号)
(4)将t2℃时a、b、c三种物质饱和溶液的降温到t1℃时,三种溶液的溶质质量分数大小关系是_____。
(5)若a中含有少量b,应用_____法提纯a。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~H 内初中化学常見物貭。己知 A 属于盐,常用作建筑材料, E 是赤铁矿石的主要成分,F 可用于改良酸性土壤, H 的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全棕标出)。
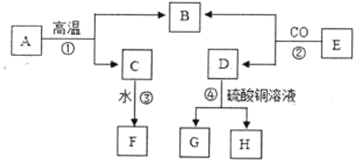
(1)写出 A、E 的化学式:A_____ ; E _____。
(2)写出反应②的化学方程式 :_____ 。
(3)用 F 改良酸性土壤的化学方程式_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究小组利用下图装置进行实验(注射器的摩擦力忽略不计)。
已知:A的容积为250 mL,B中盛有足量的水,实验前K1、K2、K3均已关闭。

(1)检查 A装置的气密性。打开 K1,向外拉注射器的活塞,松手后,观察到________,说明装置的气密性良好。
(2)测定 A 瓶气体中二氧化碳含量。打开K1,用注射器向A中注入20 mL NaOH溶液(足量),关闭K1,充分反应后,_______________(填实验操作),观察到 B 中的水进入 A 中,当B中液面不再变化时,测得B中减少了60 mL水,则A中CO2的体积分数约为______________ %。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与人类生产生活息息相关。
(1)下列物质的性质与应用关系不正确的是_____。
A 氢氧化钠能与油脂反应,在生活中可用来除油污
B 人体缺少必需微量元素会得病,应合理补充微量元素
C 中和反应生成盐和水,那么生成盐和水的反应一定是中和反应
D 熟石灰具有碱性,可用于改良酸性土壤
(2)兴趣小组的同学借助无色酚酞溶液验证氢氧化钠和盐酸确实发生了反应,反应后溶液呈无色,甲同学认为氢氧化钠与盐酸恰好完全反应,乙同学认为甲同学的说法不准确,你觉得呢?说出你的猜想,并证明_____。
(3)为探究一氧化碳还原氧化铁的实验,同学们设计如图的实验,并查阅了相关资料,仔细思考,回答下列问题。
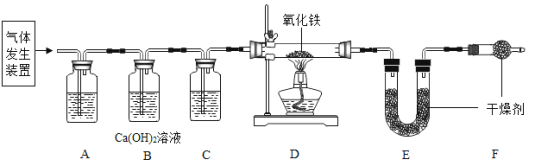
(查阅资料)草酸晶体(H2C2O43H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O43H2O CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(问题讨论)
①D装置的化学反应方程式为_____。
②进入D装置的气体是纯净、干燥的CO,则A、C装置中的试剂依次是_____、_____ (填名称)。
③请指出上述实验装置的一个明显缺陷,怎样改进实验装置_____。
(4)将10g的铜一锌合金放入试管中,向其中加入49g质量分数为20%的稀硫酸,恰好完全反应,求:①生成氢气的质量_____。②样品中锌的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用菱锰矿[主要成分为MnCO3,含FeCO3、Cu2(OH)2CO3、SiO2等杂质]为原料来制取二氧化锰,其生产流程示意图如下:
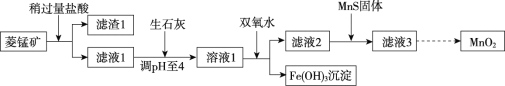
回答下列问题:
(1)将滤液与滤渣分离的操作是______。
(2)向菱锰矿中加入盐酸,MnCO3、FeCO3、Cu2(OH)2CO3都溶解并转化为MnCl2、FeCl2、CuCl2。盐酸与MnCO3反应的化学方程式为________。
(3)加入生石灰将溶液pH调至4,此时溶液呈________(填“酸性”或“碱性”)。
(4)加入双氧水将铁元素转化为Fe(OH)3沉淀,其反应为: 2FeCl2 + H2O2 + 4H2O = 2Fe(OH)3↓ + 4HCl,该反应化合价发生变化的元素是氧和_______。
(5)加入Na2S、MnS等硫化物,均可将MnCl2中混有的CuCl2转化为CuS沉淀除去,但实际生产中选用MnS,其原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某化学兴趣小组。设计的金属活动性顺序的探究实验。
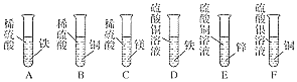
(1)上述实验中,有气泡生成的是________(填写装置序号)。
(2)试管F中出现的实验现象是______________。
(3)上述实验能否证明镁、锌、铁、铜、银五种金属的活动性强弱?____请说明理由_____。
(4)我国古代“湿法炼铜”就是利用了试管D中的反应原理,请写出该反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)下图是氧元素、铝元素在周期表中的部分信息,以及四种粒子的结构示意图。

根据图示回答下列问题:
(1)氧原子的原子核内质子数是 ,铝的相对原子质量是 ;
(2)写出甲和乙形成化合物的化学式 ;
(3)粒子B的符号为 ;
(4)D粒子中X= 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料广泛应用于生产生活中。
(1)生铁和钢都是铁的合金,合金的硬度一般比各成分金属_____
(2)厨房中的下列物品所使用的主要材料属于金属材料的是___
A 陶瓷碗 B 不锈钢炊具 C 橡胶手套 D 铜质水龙头
(3)西汉《淮南万毕术》中记载有“曾青得铁则化为铜”,曾青指的是硫酸铜溶液,该反应的化学反应方程式__
(4)工业炼铁的主要设备是高炉,写出高炉中一氧化碳跟氧化铁在高温下反应的化学方程式__
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com