
分析 (1)根据锰的活动性比铁强,所以锰的金属活动性比铜强,能与硫酸铜反应生成硫酸锰和铜进行分析;
(2)根据“加入H2SO4溶解MnCO3”,“MnSO4溶液为浅红色”,进行书写化学方程式和实验现象;
(3)利用MnCO3$\frac{\underline{\;高温\;}}{\;}$MnO+CO2↑;2MnO+O2$\frac{\underline{\;\;△\;\;}}{\;}$2MnO2,则MnCO3~MnO2,进行计算.
解答 解:(1)根据锰的活动性比铁强,所以锰的金属活动性比铜强,能与硫酸铜反应生成硫酸锰和铜,化学方程式为:Mn+CuSO4=MnSO4+Cu;
(2)因为“加入H2SO4溶解MnCO3”,“MnSO4溶液为浅红色”,所以化学方程式MnCO3+H2SO4=MnSO4+CO2↑+H2O,反应的现象是固体减少,有气泡产生,溶液变成浅红色;
(3)因为MnCO3$\frac{\underline{\;高温\;}}{\;}$MnO+CO2↑,2MnO+O2$\frac{\underline{\;\;△\;\;}}{\;}$2MnO2,
则MnCO3~MnO2,
设理论上能制得MnO2的质量为x
MnCO3~MnO2
115 87
11.5t x
$\frac{115}{11.5t}$=$\frac{87}{x}$
x=8.7t.
故答案为:
(1)Mn+CuSO4=MnSO4+Cu;
(2)MnCO3+H2SO4=MnSO4+CO2↑+H2O;固体减少,有气泡产生,溶液变成浅红色;
(3)8.7t.
点评 本题难度不大,掌握金属的化学性质、化学方程式的书写、计算是正确解答本题的关键.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
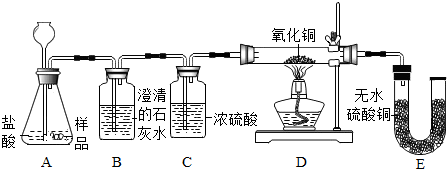
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NO | B. | N2 | C. | NO2 | D. | N2O |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
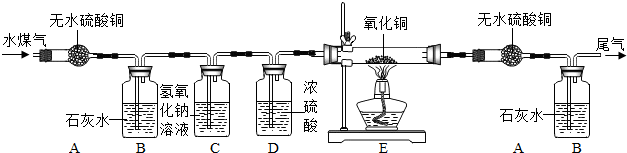
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化钙--熟石灰、消石灰 | B. | 汞--水银 | ||
| C. | 碳酸氢钠--小苏打 | D. | 氢氧化钠--烧碱、火碱、苛性钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10g碳酸钙和10g碳酸钠 | B. | 10g碳酸钙和5.6g硝酸银 | ||
| C. | 5.6g铁粉和5.6g锌粉 | D. | 2.4g镁和2.2g氧化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
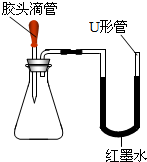 如图是某同学设计的趣味实验装置,其气密性良好.
如图是某同学设计的趣味实验装置,其气密性良好.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
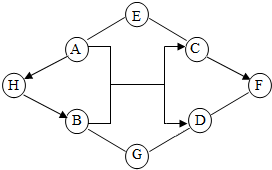 如图中A~H是初中化学常见的物质.A俗称苏打;C可用作补钙剂;G是一种常见的氮肥,含氮量为35%;H、F物质类别相同.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.
如图中A~H是初中化学常见的物质.A俗称苏打;C可用作补钙剂;G是一种常见的氮肥,含氮量为35%;H、F物质类别相同.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com