��2013?�Ͼ���ģ����1���������ϵ�ʹ��
�������������ʱ��Ҫ����ͭ��ʱ�����ö࣬����
A
A
�йأ�����ţ���
A�������Ļ�� B�������ĵ����� C�������ĵ����� D���ؿ��н���Ԫ�صĺ���
������һ��ʹ��ͭ�Ͻ���ڴ�ͭ����Ϊͭ�Ͻ���۵�Ҫ��ͭ�ͣ�Ӳ��Ҫ��ͭ
��
��
�����������
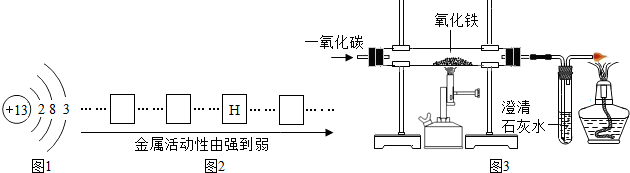
��2�������Ľṹ
ͼ1������ԭ�ӽṹʾ��ͼ���ڻ�ѧ��Ӧ����ԭ����
ʧȥ
ʧȥ
����õ�����ʧȥ�������Ӵﵽ�ȶ��ṹ����˻���������Ԫ��ͨ����
+3
+3
�ۣ�
��3�������Ļ��
���뽫ͭ�����������ֽ�����Ԫ�ط�����д�����н������˳��ͼ2�е���Ӧλ�ã�
��Ҫ�����֤ͭ���������Ļ��˳��ijͬѧ�Ѿ�ѡ���˴�ĥ������˿������Ϊ������Ҫ�������Լ���
AlCl3��CuCl2��Һ���𰸺������ɣ�
AlCl3��CuCl2��Һ���𰸺������ɣ�
��
��þ�����������ֽ���������������ϡ���ᷴӦ�����ɵ���������������Ҫ���ĵĽ��������ɶൽ�ٵ�˳����
����þ����
����þ����
��4����������ʴ
�����Ļ�Ա���ǿ�������ڿ�����ȴ���ֳ����õĿ���ʴ���ܣ���ԭ����
��������һ�����ܵ�����Ĥ
��������һ�����ܵ�����Ĥ
��
�����ڳ�ʪ�Ŀ�����������ʴ��Ϊ�˷�ֹ����Ʒ��ʴ�����dz�����
Ϳ�ͣ��𰸺������ɣ�
Ϳ�ͣ��𰸺������ɣ�
�ķ�������дһ�֣����ﵽĿ�ģ����������Ʒ����ʢ�й���ϡ�����ϴ���У��۲쵽��Һ��ƣ�һ��ʱ�������ɫ�����ݳ�����Һ��ƵĻ�ѧ��Ӧ����ʽ�ǣ�
Fe2O3+6HCl�T2FeCl3+3H2O
Fe2O3+6HCl�T2FeCl3+3H2O
��
��ͭ����Ҳ���������ͭ�̣�����Ҫ�ɷ��Ǽ�ʽ̼��ͭ[Cu
2��OH��
2CO
3]��ͭ���������������ˮ�й��⣬��������е�
CO2
CO2
�йأ�
��5��������ұ��
������ʱ���ҹ����Ͷ������ַ����ˡ�ʪ����ͭ�����������������Ϊͭ�����÷�Ӧ����ʽ��ʾ��ұ��ԭ��
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
_��
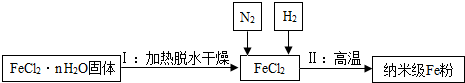
��С��ͬѧ����ʵ������ͼ3��ʾװ��ģ�ҵ����������ݴ˻ش�
ʵ���в������ڵ�����Ϊ��
��ɫ������ɫ
��ɫ������ɫ
����Ӧ�Ļ�ѧ����ʽ��
��
��ijͬѧʵ����ɺ��ֹ����ij���ʯ��ˮ����0.88g�����ͬѧͨ��װ�õ�CO��������һ��Ҫ����
0.56g
0.56g
g������С�������λ����