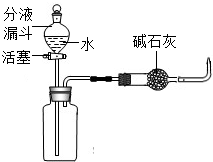
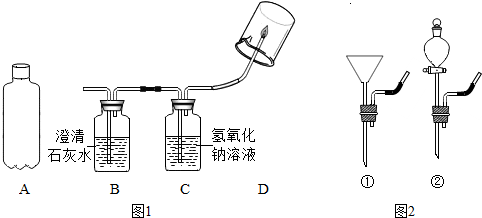
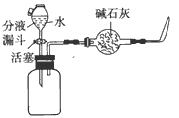
解:【实验和结论】(1)将装满水的集气瓶倒置于水中的气泡上方接收气体,该方法称为排水集气法;
(2)澄清石灰水变浑浊,说明气体中含有二氧化碳,与猜想I所猜测相符,因此猜想I成立;在点燃条件下,甲烷在氧气中完成燃烧生成二氧化碳和水,该反应的化学方程式可表示为CH
4+2O
2
CO
2+2H
2O;甲烷具有可燃性,但具有可燃性的气体并非只有甲烷,因此,由可燃判断气体为甲烷不够具有说服力;
(3)利用含氢元素可燃物燃烧后可生成水,因此采取用干冷(或用无水粘胶粘有硫酸铜的)烧杯罩于火焰上方,如果烧杯内壁出现水雾(或无水硫酸铜由白色变为蓝色),则说明这种气体含有氢;干燥管中的碱石灰由能吸收水分的氧化钙和既能吸收水又能吸收二氧化碳的氢氧化钠混合而成,在实验中起到吸收原气体中的CO
2和水蒸汽的作用;
【拓展】通过以上定性的实验仅能得到由C、H元素组成的结论,要确切得到该气体为甲烷还需要对气体中氢和碳元素的质量进行测定;
故答案为:
【实验和结论】
(1)排水集气法;
(2)成立;CH
4+2O
2
CO
2+2H
2O;能然烧的气体不一定是CH
4[或没有检验可燃性气体中的C和H的存在,合理表述均给分];
(3)②用干冷(或用无水粘胶粘有硫酸铜的)烧杯罩于火焰上方,如果烧杯内壁出现水雾(或无水硫酸铜由白色变为蓝色),则说明这种气体含有氢;吸收原气体中的CO
2和水蒸汽;
【拓展】定量测定气体中碳和氢的质量[或先用烧碱或生石灰吸收气体中的CO
2,然后用干燥剂干燥气体后测气体的密度;或将气体燃烧后生成的气体分别用浓硫酸、用碱石灰吸收,再称量浓硫酸和碱石灰的增加的质量,计算].
分析:【实验和结论】(1)根据所采取收集气体的操作方法,判断这种集气方法;
(2)根据实验现象,对气体组成的可能进行推断,判断猜想是否成立,并根据物质的变化规律,写出反应的化学方程式;由物质性质推断气体的可能性,并评价猜想;
(3)根据燃烧规律,简述检验可燃物中含有氢元素的操作方法,并根据对装置作用的认识,说明干燥管中药品在实验中所起的作用;
【拓展】根据定性测定只能得到可燃物的组成,而定量测定才能确定物质的构成,因此为判断可燃物的构成,实验中还需要相关质量的测定.
点评:可燃物在氧气中完全燃烧时,可燃物中碳元素全部生成二氧化碳,可燃物中氢元素全部生成水;检验生成物或测定生成物的质量可判断可燃物的组成及组成元素质量关系.

 CO2+2H2O;甲烷具有可燃性,但具有可燃性的气体并非只有甲烷,因此,由可燃判断气体为甲烷不够具有说服力;
CO2+2H2O;甲烷具有可燃性,但具有可燃性的气体并非只有甲烷,因此,由可燃判断气体为甲烷不够具有说服力; CO2+2H2O;能然烧的气体不一定是CH4[或没有检验可燃性气体中的C和H的存在,合理表述均给分];
CO2+2H2O;能然烧的气体不一定是CH4[或没有检验可燃性气体中的C和H的存在,合理表述均给分];

 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案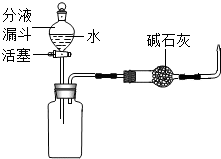 水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分.请你与他们一起完成如下的探究:
水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分.请你与他们一起完成如下的探究: