
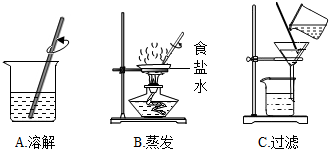
分析 (1)粗盐的主要成分是氯化钠,粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析解答.
(2)操作B是蒸发操作,结合玻璃棒的作用,进行分析解答.
(3)NaCl的产率偏低,可能是由于氯化钠质量减少或水的质量偏多造成的,据此进行分析判断即可.
解答 解:(1)粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),正确的操作顺序是③②⑤.
(2)操作B是蒸发操作,用玻璃棒不断搅拌的目的是防止局部温度过高,造成液体飞溅.
(3)A、过滤时滤纸有破损,造成有一部分不溶性的泥沙等进入滤液,会导致所得精盐质量偏大,产率偏高,故选项错误.
B、蒸发时有固体溅出,会造成原混合物中的食盐没有全部转到精盐中,导致所得精盐质量偏小,产率偏低,故选项正确.
C、称量时,少量晶体仍粘在蒸发皿上,会造成原混合物中的食盐没有全部转到精盐中,导致所得精盐质量偏小,产率偏低,故选项正确.
D、溶解粗盐时,加入的水量不足,会导致食盐有一部分没被溶解,造成原混合物中的食盐没有全部转到精盐中,导致所得精盐质量偏小,产率偏低.
故答案为:(1)ACB;(2)防止局部温度过高,造成液体飞溅;(3)BCD.
点评 本题难度不大,掌握粗盐提纯的实验原理与实验步骤、NaCl的产率偏低的原因等是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)称取上述固体样品8g溶于100mL水配成溶液,向溶液中滴加过量的氯化钙溶液充分反应后,静置. | 产生白色沉淀① | 说明久置固体中,一定含有Na2CO3 |
| (2)用玻璃棒蘸取少量①中的上层清液滴在pH试纸上,与标准比色卡对比,测出pH | pH=10 | 说明固体中,还一定含有 ②NaOH(填化学式). |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 1将NaOH溶液稀释,滴人该酚酞溶液. | 溶液变红,继续滴加酚酞溶液,红色消失 | 甲同学猜想不正确 (填“正确”或“不正确”) |
| 2向澄清石灰水中滴入该酚酞溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
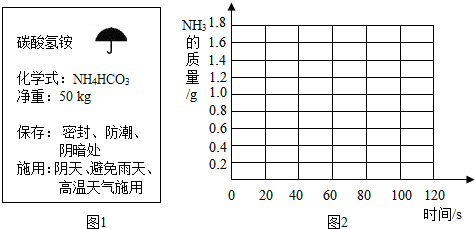
| 时间/S | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加质量/g | 0 | 0.7 | 1.0 | m | 1.5 | 1.6 | 1.7 | 1.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com