
分析 对于该题我们可以通过其溶解度的有关知识完成,因为形成镉的沉淀后还有极少量的镉离子存在于水中,所以该问题就转化为利用溶解的沉淀求出镉的质量,据此分析解答即可.
解答 解:设取1L这样的河水(1kg),加适量的氢氧化钠使其中的镉全部变成Cd(OH)2,此时少量的该沉淀溶解,成为此时该沉淀的饱和溶液,则依据此时该物质的溶解度可知1kg河水可溶解的Cd(OH)2质量为1.7×10-4×$\frac{1000g}{100g}$=1.7×10-3 g,其中溶解的Cd2+离子的质量为1.7×10-3g×$\frac{112}{146}$=1.3 mg;
溶解极少量的溶质基本不改变溶液体积,故这1L河水中Cd2+的浓度为1.3mg/L.
类似的做法可知类似,饱和CdCO3的溶液中Cd2+浓度为2.8×10-6×10×$\frac{112}{172}$g/L=0.018mg/L,加碳酸钠仍不能达标.
故答案为:Cd(OH)2:1.3 mg/L>0.005 mg/L不符合;CdCO3:0.018 mg/L>0.005 mg/L不符合.
点评 此题是一道溶解度计算的变形题,解题的关键是能够利用溶解度的数值对溶解的离子质量的计算.


科目:初中化学 来源: 题型:选择题
| A. | 用氢氧化钡溶液区分硫酸铵、硫酸镁和硝酸铜 | |
| B. | 用碳酸钠和氢氧化钙制备氢氧化钠 | |
| C. | 用氢氧化钠溶液和浓硫酸除去二氧化碳中的氯化氢和水蒸气 | |
| D. | 用氢氧化钙溶液除去氢氧化钠溶液中的碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子很小 | B. | 分子是可分的 | ||
| C. | 分子之间有间隔 | D. | 分子总在不断地运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
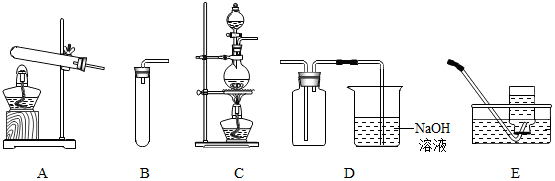
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
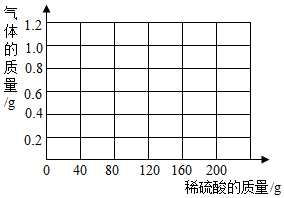 镁带在空气中放置一段时间表面会氧化,其中所含的其它杂质与稀硫酸不反应.为了测定某种镁带中镁的质量分数,某实验小组进行如下实验:先用细砂纸打磨镁带表面,使用精密天平称取打磨后11.25克镁带样品放在烧杯中,每次加入40.00克稀硫酸(不考虑水的挥发)使充分反应,测量反应前后装置连同内盛物质的质量.
镁带在空气中放置一段时间表面会氧化,其中所含的其它杂质与稀硫酸不反应.为了测定某种镁带中镁的质量分数,某实验小组进行如下实验:先用细砂纸打磨镁带表面,使用精密天平称取打磨后11.25克镁带样品放在烧杯中,每次加入40.00克稀硫酸(不考虑水的挥发)使充分反应,测量反应前后装置连同内盛物质的质量.| 加入稀硫酸次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯和所称物质总质量(克) | 120.15 | 159.95 | 199.75 | 239.55 | 279.45 | 319.45 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
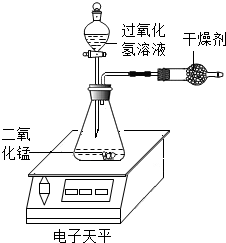 某化学兴趣小组对过氧化氢分解生成水和氧气的条件进行探究,请你参与.
某化学兴趣小组对过氧化氢分解生成水和氧气的条件进行探究,请你参与.| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| H2O2溶液浓度 | 5% | 5% | 5% | 10% | 10% | 30% | 30% |
| MnO2粉末(g) | 1.0 | 0.8 | 0.6 | 0.6 | 0.4 | 0.4 | 0.2 |
| 所用的时间(s) | 205 | 205 | 220 | 80 | 90 | 3 | 4 |
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 | 120 | 140 | 160 | 180 | 200 |
| 示数(g) | 565.40 | 565.37 | 565.34 | 565.30 | 565.28 | 565.26 | 565.24 | 565.23 | 565.22 | 565.21 | 565.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
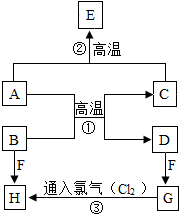 A〜H 初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G-H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:
A〜H 初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G-H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com