
| 操作序号 | 1 | 2 | 3 | 4 |
| 剩余固体质量/(g) | 4.25 | 3.95 | 3.35 | 3.35 |
分析 根据质量守恒定律可知,固体的质量变化量为生成的二氧化碳的质量,即二氧化碳的质量为2.2g.根据二氧化碳求算碳酸钙和氧化钙,进而根据要求求算质量分数
解答 解:根据质量守恒定律,生成的二氧化碳的质量为5.55g-3.35g=2.2g
设碳酸钙的质量为x,生成的氧化钙的质量为y.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56 44
x y 2.2g
$\frac{100}{x}$=$\frac{56}{y}$=$\frac{44}{2.2g}$
x=5g
y=2.8g
石灰石样品中碳酸钙的质量分数$\frac{5g}{5.55g}$×100%≈90%
产品中生石灰的质量分数为$\frac{2.8g}{3.35g}$×100%≈84%
答:(1)完全反应后生成的CO2质量是 2.2g.
(2)石灰石样品中碳酸钙的质量分数是 90%
(3)产品中生石灰的质量分数是 84%
点评 根据质量守恒定律计算时首先要确定有效的数据,纯净物可以用于计算,混合物的质量不可以用于化学方程式的计算.


科目:初中化学 来源: 题型:实验探究题
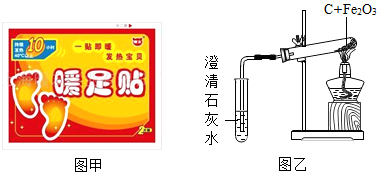 “暖足贴”利用铁氧化生锈时会放热的原理从而达到给人局部热敷的作用,具有一贴即热,快速热敷的作用,深受大众的喜爱.图甲是某品牌“暖足贴”的图片.A、B两小组的同学,通过查阅资料发现,其主要成份为:铁粉、活性炭、水、食盐等物质.
“暖足贴”利用铁氧化生锈时会放热的原理从而达到给人局部热敷的作用,具有一贴即热,快速热敷的作用,深受大众的喜爱.图甲是某品牌“暖足贴”的图片.A、B两小组的同学,通过查阅资料发现,其主要成份为:铁粉、活性炭、水、食盐等物质.| 铁的氧化物 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红色 | 黑色 | 黑色 |
| 化学性质 | 可溶于稀硫酸 | 常温下不溶于稀硫酸 | 可溶于稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
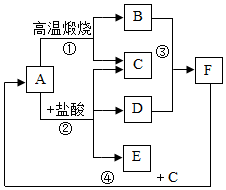 A、B、C、D、E、F为初中化学常见物质,他们之间的转化如图所示,A是固体物质,C是可以促进植物光合作用的气体,请回答下列问题:
A、B、C、D、E、F为初中化学常见物质,他们之间的转化如图所示,A是固体物质,C是可以促进植物光合作用的气体,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(克) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(克) | 4.0 | 2.0 | 0.6 | 0.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 除去CO2中CO--通入氧气点燃 | |
| B. | 除去N2中的O2--通过灼热铜网 | |
| C. | 除去生石灰中混有的少量碳酸钙--将混合物溶于水后过滤 | |
| D. | 除去铁粉中混有的少量铜--加入适量稀盐酸充分反应后过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 工业上可以利用分离液态空气的方法制取氧气 | |
| B. | 氧气可以支持燃烧,说明氧气具有可燃性 | |
| C. | 氧气供给呼吸,它和体内物质发生氧化反应,释放能量 | |
| D. | 干冰可用于人工降雨,是因为干冰升华时吸收大量的热 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com