
(8分)氯化钙是重要的化工原料。某工业碳酸钙所含的杂质主要是氧化铁及
一些不与酸碱反应的难溶性物质,以这种工业碳酸钙为原料生产氯化钙的主要流程如下图
所示: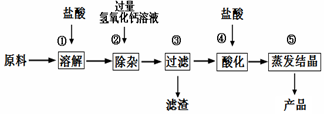
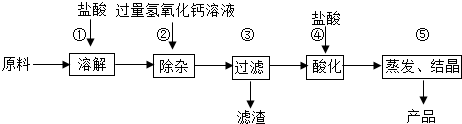
(1)用化学方程式表示由碳酸钙生成氯化钙的反应原理: 。
(2)步骤③得到的滤渣含有氢氧化铁,请写出步骤②发生复分解反应生成氢氧化铁的化学方程式: 。
(3)步骤④加入盐酸的目的是除去 ;步骤⑤利用盐酸的 性质,除去过量的盐酸。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
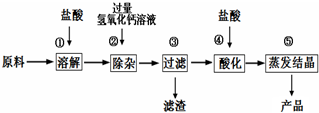
(8分)氯化钙是重要的化工原料。某工业碳酸钙所含的杂质主要是氧化铁及
一些不与酸碱反应的难溶性物质,以这种工业碳酸钙为原料生产氯化钙的主要流程如下图
所示:
(1)用化学方程式表示由碳酸钙生成氯化钙的反应原理: 。
(2)步骤③得到的滤渣含有氢氧化铁,请写出步骤②发生复分解反应生成氢氧化铁的化学方程式: 。
(3)步骤④加入盐酸的目的是除去 ;步骤⑤利用盐酸的 性质,除去过量的盐酸。
查看答案和解析>>
科目:初中化学 来源:2011年初中毕业升学考试(福建厦门卷)化学 题型:填空题
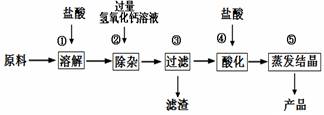
(8分)氯化钙是重要的化工原料。某工业碳酸钙所含的杂质主要是氧化铁及
一些不与酸碱反应的难溶性物质,以这种工业碳酸钙为原料生产氯化钙的主要流程如下图
所示:
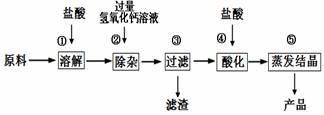
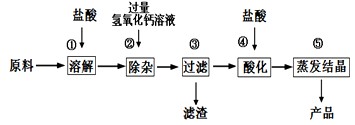
(1)用化学方程式表示由碳酸钙生成氯化钙的反应原理: 。
(2)步骤③得到的滤渣含有氢氧化铁,请写出步骤②发生复分解反应生成氢氧化铁的化学方程式: 。
(3)步骤④加入盐酸的目的是除去 ;步骤⑤利用盐酸的 性质,除去过量的盐酸。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:福建省中考真题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com