

分析 (1)根据铁矿石的成分和氧化物的定义分析;
(2)①根据铜的性质和用途分析回答;
②根据稀硫酸与氧化铁的反应,写出该反应的化学方程式.
(3)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此分析回答有关的问题.
解答 解:(1)赤铁矿、磁铁矿的主要成分分别是Fe2O3、Fe3O4,均是由两种元素组成的且有一种是氧元素的化合物,均属于氧化物.
(2)①汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和导电性.
②焊接铁制品时,通常先用稀硫酸除去其表面的铁锈,铁锈的主要成是氧化铁,该反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(3)Ⅰ.A、铁和铜都不与硫酸锌反应,说明铁和铜在锌的后面,无法说明铁和铜的关系,故A错误;
B、锌与硫酸亚铁溶液反应生成硫酸锌和铁,说明锌在铁的前面,铜与硫酸亚铁溶液不反应,说明铁在铜的前面,从而说明锌>铁>铜,故B正确;
C、铁与硫酸锌溶液不反应,说明锌在铁的前面,铁与硫酸铜溶液反应生成硫酸亚铁和铜,说明铁在铜的前面,从而说明锌>铁>铜,故C正确;
D、锌、铁都能与稀硫酸反应且锌反应的速率比铁快,说明金属活动性锌的大于铁,铜不与硫酸反应,说明铜位于氢的后面,从而说明锌>铁>铜,故C正确;
Ⅱ.在金属活动性顺序中,锌>氢>铜>银,向AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粉,锌能先与硝酸银反应生成银和硝酸锌,当硝酸银完全反应后再与硝酸铜反应生成铜和硝酸锌,充分反应后过滤,得到滤渣和滤液.
①若滤液呈无色,说明了溶液中的硝酸铜完全发生了反应,则滤渣中一定含有的物质是Ag、Cu,可能有剩余的锌;
②若向滤渣中滴加稀盐酸,无气泡产生,说明了没有剩余的锌,当锌只能部分置换银时,则滤液中所含溶质的成分是:硝酸银、硝酸铜和硝酸锌;当锌恰好置换出银或只能部分置换部分铜时,则滤液中所含溶质的成分是:硝酸铜和硝酸锌;当锌恰好置换出铜时,则溶液的中溶质只有硝酸锌.所以滤液中所含溶质的成分可能有三种情况.
故答为:(1)AD;(2)①导电.②Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.(3)Ⅰ.BC.Ⅱ.①Ag、Cu;②三.
点评 同学们要会利用金属活动顺序表设计实验,去验证金属的还原性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.


 口算题天天练系列答案
口算题天天练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 普通汽车施用的燃料是汽油或柴油,汽车尾气中的含铅化合物、氮的氧化物以及一氧化碳等(填一种)会对空气造成污染.
普通汽车施用的燃料是汽油或柴油,汽车尾气中的含铅化合物、氮的氧化物以及一氧化碳等(填一种)会对空气造成污染.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
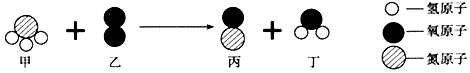
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图表示一定质量的KClO3和MnO2固体混合物在受热过程中各物质质量随时间的变化趋势.下列说法不正确的是( )
如图表示一定质量的KClO3和MnO2固体混合物在受热过程中各物质质量随时间的变化趋势.下列说法不正确的是( )| A. | d是二氧化锰 | |
| B. | b是氧气,c是氯化钾 | |
| C. | t1时反应开始发生 | |
| D. | t1和t2时,固体中钾元素质量保持不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | CaO(CaCO3) | 加水溶解、过滤 |
| B | NaOH溶液(Na2SO4) | 加入过量的Ba(OH2)溶液、过滤 |
| C | CO(CO2) | 通过足量氢氧化钠溶液,并干燥 |
| D | CuSO4溶液(H2SO4) | 加入足量的铜粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
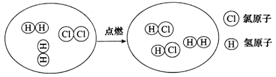
| A. | 该反应属于化合反应 | |
| B. | 反应前后分子的种类发生了改变 | |
| C. | 反应前后各元素的质量不变 | |
| D. | 参加反应的H2和Cl2的分子个数比为2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com