
| A. | 加入稀盐酸,有无色气体产生的物质中一定有碳酸盐 | |
| B. | 经点燃,产生蓝色火焰的气体不一定是一氧化碳 | |
| C. | 能使紫色石蕊试液变红的一定是酸 | |
| D. | 用燃着的木条深入某气体中,火焰熄灭,则该气体一定是二氧化碳 |
分析 A、根据酸的化学性质进行分析判断.
B、根据常见气体燃烧的火焰进行分析判断,
C、使紫色石蕊试液变红的不一定酸;
D.用燃着的木条伸入某气体中,火焰熄灭,说明该气体不能燃烧、不能支持燃烧.
解答 解:A、加入稀盐酸,有无色气体产生的物质中不一定含有碳酸盐,也可能是活泼金属、碳酸氢盐等,故选项说法错误.
B、经点燃,产生蓝色火焰的气体不一定是一氧化碳,也可能是甲烷等气体,故选项说法正确.
C、使紫色石蕊试液变红的显酸性,不一定是酸;故选项说法错误.
D.用燃着的木条伸入某气体中,火焰熄灭,说明该气体不能燃烧、不能支持燃烧,则该气体不一定是二氧化碳,也可能是氮气等不能支持燃烧的气体,故选项说法错误.
故选B.
点评 本题难度不大,掌握酸的化学性质、常见气体的性质与检验方法等是正确解答本题的关键.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:初中化学 来源: 题型:解答题

| 步骤 | 操作 | 主要现象 | 结论 |
| Ⅰ | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引 | 部分固体被吸引 到磁铁上 | 可能有Fe或Fe3O4 |
| Ⅱ | 取滤纸上的剩余固体少量,放入图2所示的 试管a中,通入氧气,用酒精灯加热. | 固体剧烈燃烧,b中溶液变浑浊 | 一定有C |
| Ⅲ | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸. | 无明显现象 | FeO和Fe2O3 |
| Ⅳ | 取步骤 I 磁铁上的固体少量,放入试管中,逐滴加入稀盐酸. | 产生气泡 | 一定有Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2H2O→2H2↑+O2↑ | B. | H2SO4+NaOH→NaSO4+H2O | ||
| C. | Fe+HCl→FeCl2+H2↑ | D. | Ca(HCO3)2$\stackrel{△}{→}$CaCO3↓+CO2↑+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
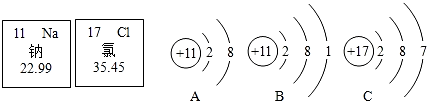
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
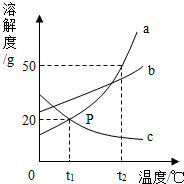 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:(1)P点的含义是t1℃时a与c的溶解度相等.
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:(1)P点的含义是t1℃时a与c的溶解度相等.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5 g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.lg | I2.7g |
| 性质 | Na2CO3 | NaHCO3 | 性质比较 |
| 溶液的酸碱性 | 碱性 | 碱性 | 相铜条件下,Na2C03溶液的碱性更强 |
| 热稳定性 | 稳定 | 不稳定 | NaHCO3受热分解生成Na2C03、C02 和H20 |
| 与盐酸反应 | 反应 | 反应 | 均产生CO2,但NaHCO3与盐酸的反应更加剧烈 |
| 实验方案 | 实验现象及结论 1 |
| 方案一:20℃时,在100 g水中加入11 g该白色固体,充分溶解 | 若有白色固体剩余,样品为碳酸氢钠; 否则为碳酸钠. |
| 方案二:分别将两种待测固体溶于水制成5%的溶液,用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象 | pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液. |
| 方案三:分别取少量固体于試管中加热,将产生的气体通入澄清的石灰水中. | 若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠. |
| 方案四:如阁所示,分别将气球中的白色固体全部且同时倒入装有盐酸的试管中,观察现象. | 气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠 |
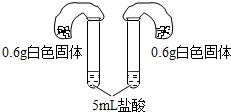 【实验反思】
【实验反思】查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO2:“2”表示一个二氧化硫分子含有两个氧原子 | |
| B. | 2N:“2”表示两个氮元素 | |
| C. | $\stackrel{+2}{Mg}$O:“+2”表示氧化镁中镁元素的化合价为+2价 | |
| D. | 2NO3-:“2”表示两个硝酸银离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
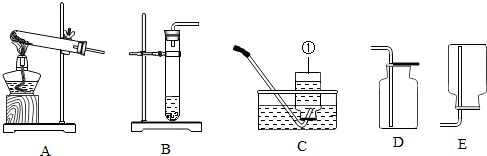
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com