
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | 2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑ | ||
| C. | CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| E. | CuO+2HCl═CuCl2+H2O | F. | NaOH+HCl═NaCl+H2O |
分析 根据习题中信息可知元素的化合价发生了变化的反应是氧化还原反应,则若在反应中各元素的化合价都没有变化,则不属于氧化还原反应.
解答 解:A、Mg元素的化合价从0升高到+2价,O元素的化合价从0降低到-2价,有化合价的变化,属于氧化还原反应,故A正确;
B、Cl元素的化合价从+5降到-1,O元素的化合价从-2升高到0,有化合价的变化,属于氧化还原反应,故B正确;
C、反应中Ca、H、O三种元素的化合价都没有变化,则不属于氧化还原反应,故C错误;
D、H元素的化合价从0升高到+1,Cu元素的化合价从+2降低到0,有化合价的变化,属于氧化还原反应,故D正确;
E、反应中Cu、H、O、Cl四种元素的化合价都没有变化,则不属于氧化还原反应,故E错误;
F、反应中Na、H、O、Cl四种元素的化合价都没有变化,则不属于氧化还原反应,故F错误.
故选:ABD.
点评 本题属于信息习题,学生应能利用信息结合化合价的判断来分析反应类型的判断,注意知识的灵活使用来解答.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
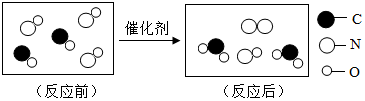 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的小球代表不同原子.下列说法正确的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的小球代表不同原子.下列说法正确的是( )| A. | 此反应有单质参加 | |
| B. | 此法可以有效减少温室效应 | |
| C. | 生成物全部是化合物 | |
| D. | 参加反应的两种分子的个数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
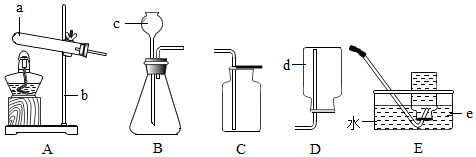
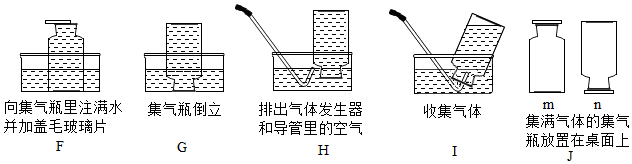
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
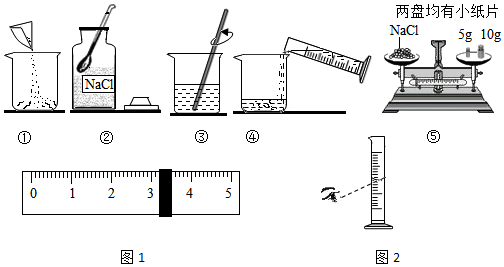
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
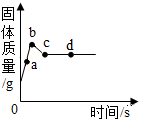 金属具有广泛的应用.
金属具有广泛的应用.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
| 剩余固体质量/g | 34.2 | 33.4 | 32.6 | 31.8 | 31.8 |
查看答案和解析>>
科目:初中化学 来源:2016届山东省临沂市生素质教育特长展示测评化学试卷(解析版) 题型:选择填充题
下面右图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,下表中符合图示关系的是
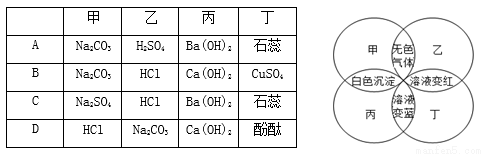
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com