
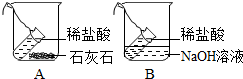
 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究.
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究.分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答 解:(1)提出假设:化学反应中,反应物的总质量与生成物的总质量相等.
故填:相等.
(4)小洁的结论正确的,导致另一种结论错误的原因是:反应生成的二氧化碳逸散到空气中.
故填:小洁;反应生成的二氧化碳逸散到空气中.
(5)从原子的角度可知,化学反应前后,原子的种类、总个数不变,原子的质量不变,因此反应前后质量不变.
故填:化学反应前后,原子的种类、总个数不变,原子的质量不变.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
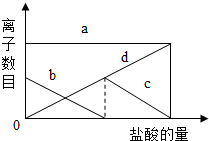 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:| A. | a:K+; b:CO32-; c:HCO3-; d:Cl- | |
| B. | a:K+; b:CO32-; c:Cl-; d:HCO3- | |
| C. | a:Cl-; b:K+; c:CO32-; d:HCO3- | |
| D. | a:K+; b:HCO3-; c:Cl-; d:CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
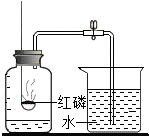 下面是测定空气中氧气体积分数的实验.在集气瓶内预先装少量水,余下的容积5等分,做好标记,在带橡皮塞和导管的燃烧匙内装足量的红磷,用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入集气瓶内,塞紧橡皮塞(如图).待红磷熄灭并冷却到室温后,打开弹簧夹.
下面是测定空气中氧气体积分数的实验.在集气瓶内预先装少量水,余下的容积5等分,做好标记,在带橡皮塞和导管的燃烧匙内装足量的红磷,用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入集气瓶内,塞紧橡皮塞(如图).待红磷熄灭并冷却到室温后,打开弹簧夹.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在溶洞中,当溶有Ca(HCO3)2的水液发生分解,析出固体(在洞顶或洞底),日久天长便形成了钟乳石 | |
| B. | 长期盛放NaOH溶液的试剂瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气压小于瓶外大气压的缘故 | |
| C. | “通风橱”是利用排风扇将橱内废气直接排放到室外的装置,它是种非常完善的防污设施 | |
| D. | 高压氧舱可治疗煤气中毒,原因是和血红蛋白结合的CO跟氧气反应生成无毒的CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 | 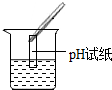 | 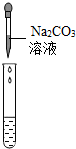 | 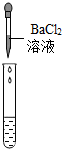 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生无色气泡有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
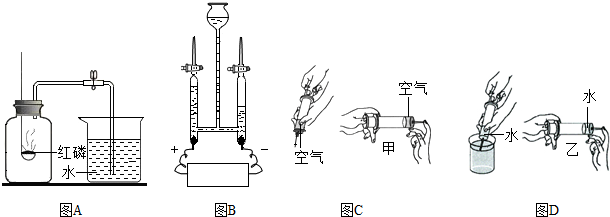
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
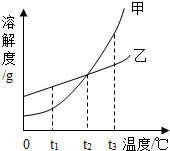
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com