��2012?��������ģ���������º�1.01��10
5Pa�����²ⶨþ��ԭ��������������ͼ������������ʢ��þ���ĸ�����С�ף����һ��ʵ��װ�ã�ÿ������ֻ������һ�Σ���
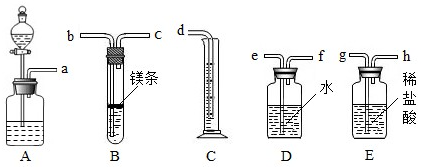
��ش��������⣺
��1���������������������ң���������Ľӿ����ӵ��Ⱥ�˳��Ϊa��
g
g
��
h
h
��b��c��f��e��d����д��ĸ����
��2��װ��A�еķ�Һ©����ʢ�ŵ�Һ����
ˮ
ˮ
��������
ʹAƿ�е��������Eƿ������Eƿ�е���ѹ����ϡ����ѹ��Bװ����Mg������ѧ��Ӧ
ʹAƿ�е��������Eƿ������Eƿ�е���ѹ����ϡ����ѹ��Bװ����Mg������ѧ��Ӧ
��
��3������������Ҫ���еIJ������������¼�����
�ٴ�����B�е����ʻָ�������ʱ��������ͲC��ˮ����������轫�ⶨ���������ɱ�״����ΪVmL����
�ڲ���þ�����������Ĥ������������ƽ�ϳ���������������Ϊmg����������Ͷ���Թ�B �У�
�ۼ���װ�õ������ԣ�
����������A�Ϸ�Һ©���Ļ�������þ����ȫ�ܽ�ʱ�ٹرջ�����
���������������Ⱥ�˳����
�ۢڢܢ�
�ۢڢܢ�
��
��4����δ���Թ�B��ȴ�����¾Ͳ�����ͲC��ˮ��������⽫��ʹ����þ�����ԭ�����������ݣ���ƫ�ߡ�ƫ�ͺ���Ӱ�죩
ƫ��
ƫ��
��
��5����δ����þ����������Ĥ�ͽ���ʵ�飬�⽫��ʹ����þ�����ԭ�����������ݣ���ƫ�ߡ�ƫ�ͺ���Ӱ�죩
ƫ��
ƫ��
��
��6���ס��ҡ�����λͬѧ����ͼװ�����ⶨһ��������þ��ȫ��Ӧ�����������������
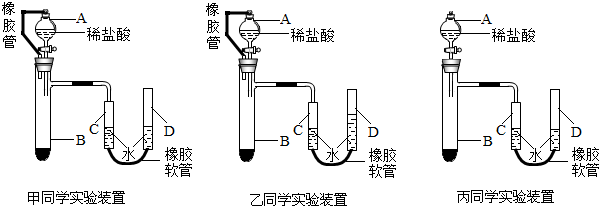
ʵ�鲽�����£�
1���װ�õ������ԣ�
�����Թ�B�м���þ����
��ȷ��������¼C��Һ��̶ȣ�CΪ���п̶ȵ������ܣ�DΪ�������ƶ���ˮ�ܣ���
����A��B�еμ�ϡ������������
��B�в���������������ָ������º�ȷ��������¼C��Һ��̶ȣ�����õ���������ΪVml
��ͬѧ����װ�������Եķ��������Ӻ�װ�ã���D��עˮ��C��D����Һ���γɸ߶Ȳ���ñ�ǣ�һ��ʱ������߸߶Ȳ�
����
����
����������С�����䡱����˵�����������ã�Ϊʹ��õ������������ȷ����¼C��Һ��̶�ʱ����ʹ�����밼Һ�����ʹ���ƽ�����������⣬��Ӧ
����D�ܣ�ʹCD����Һ����ƽ
����D�ܣ�ʹCD����Һ����ƽ
��
��ͬѧ��Ϊþ����ʵ��ǰӦ��ĥ��Ŀ����
��ȥ���������þ
��ȥ���������þ
��
��ͨ��ʵ��ǰ�����ҩƷ���������ʵ������У���������������㣬Ӧ��;���ỹ������ʵ�飺
����ʵ��
����ʵ��
��������
��;�����ʹ�������
��;�����ʹ�������
��
�����������ҡ�����λͬѧ����ʵ��װ�ã��ڲ���ݶ���ʱ�������ȶ�״̬ͼ�����ʵ����������Ӱ���ǣ��������ಽ�������Ҳ���ȷ������
ƫС
ƫС
����
ƫ��
ƫ��
���ƫ����ƫС������Ӱ�족����









