
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
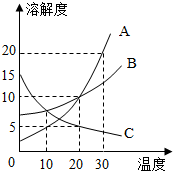 如图A、B、C三种固体物质的溶解度曲线.请回答以下问题:
如图A、B、C三种固体物质的溶解度曲线.请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ag+、Cu2+、Zn2+ | B. | Ag+、Cu2+、Zn2+、Fe2+ | ||
| C. | Cu2+、Zn2+ | D. | Zn2+、Fe2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 甲 | 乙 | 丙 | |
| 所取食盐水的质量/g | 100 | 50 | 50 |
| 加入AgNO3溶液的质量/g | 50 | 50 | 75 |
| 反应后所得沉淀物的质量/g | 1.435 | 1.435 | 1.435 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 尿素[CO(NH2)2]是一种氮肥,但尿素溶液也可用作柴油汽车尾气处理液.右图为某公司生产的一瓶车用尿素溶液的标签,用尿素溶液处理汽车尾气(含NO)时的化学方程式如下(反应条件略去):2CO(NH2)2+4NO+O2=2CO2+4N2+4H2O.
尿素[CO(NH2)2]是一种氮肥,但尿素溶液也可用作柴油汽车尾气处理液.右图为某公司生产的一瓶车用尿素溶液的标签,用尿素溶液处理汽车尾气(含NO)时的化学方程式如下(反应条件略去):2CO(NH2)2+4NO+O2=2CO2+4N2+4H2O.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ.取少量黑色产物加入到装有足量FeCl3溶液的烧杯中,充分反应后过滤,对过滤所得固体用蒸馏水洗涤. | 黑色固体部分溶解 | 猜想2和4都不成立 |
| Ⅱ.取少量黑色产物加入到装有足量稀盐酸的烧杯中,充分反应后,向溶液中滴加KSCN溶液 | 黑色固体全部溶解,溶液不变红色 | |
| Ⅲ.另取少量黑色产物装入玻璃管中,通入CO,一段时间后加热,并将反应后的气体通入装有一定量的澄清石灰水的烧杯中. | 澄清石灰水变浑浊 | 猜想1不成立 猜想3成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com