
 如图是甲、乙两种固体物质的溶解度曲线图
如图是甲、乙两种固体物质的溶解度曲线图 ×100%可知:溶解度相等则溶质的质量分数相等,t1℃时AB的溶解度相等,所以A、B两种物质的饱和溶液溶质的质量分数A=B;将t1℃的A、B两种物质的饱和溶液升温到t2℃时,其溶液中溶质、溶剂的质量不变,故所得溶液中溶质质量分数的关系为A=B;
×100%可知:溶解度相等则溶质的质量分数相等,t1℃时AB的溶解度相等,所以A、B两种物质的饱和溶液溶质的质量分数A=B;将t1℃的A、B两种物质的饱和溶液升温到t2℃时,其溶液中溶质、溶剂的质量不变,故所得溶液中溶质质量分数的关系为A=B; ×100%=37.5%;
×100%=37.5%;

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:
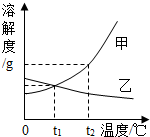 (2013?市中区一模)水是生命之源,生产之要,生活之基.泉城市民更要珍惜水、节约水、保护水.请完成下列问题:
(2013?市中区一模)水是生命之源,生产之要,生活之基.泉城市民更要珍惜水、节约水、保护水.请完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
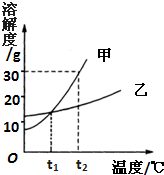 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com