
”¾ĢāÄæ”æĻĀĶ¼ŹĒ¼×”¢ŅŅ”¢±ūČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻß”£øł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
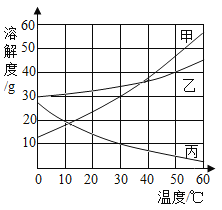
(1)30”ꏱ£¬¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹµÄČܽā¶ČÓɓ󵽊”µÄĖ³ŠņŹĒ____£»
(2)µ±¼×ÖŠ»ģÓŠÉŁĮæµÄŅŅŹ±£¬æɲÉÓĆ____·½·ØĢį“æ¼×£»
(3)30”ꏱ£¬½«10g¼×ĪļÖŹ¼ÓČėµ½Ź¢ÓŠ50gĖ®µÄÉÕ±ÖŠ£¬³ä·ÖČܽāŗó£¬ĖłµĆČÜŅŗŹĒ____£ØĢī”°±„ŗĶ”±»ņ”°²»±„ŗĶ”±£©ČÜŅŗ£»
(4)50”ꏱ£¬·Ö±šÅäÖĘ¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹµÄ±„ŗĶČÜŅŗø÷100g£¬ĖłŠčĖ®µÄÖŹĮæ×īÉŁµÄŹĒ____£ØĢī”°¼×”±”¢”°ŅŅ”±»ņ”°±ū”±£©£»
(5)20”ę£¬ÅäÖĘŅ»¶ØĮæ±ūĪļÖŹµÄČÜŅŗ£¬½«ČÜŅŗÉżĪĀµ½40”ę£¬ŹĒ·ńÓŠ¹ĢĢåĪö³ö£æ____£ØĢī”°ÓŠ”±£¬”°Ć»ÓŠ”±»ņ”°²»Č·¶Ø”±£©”£
”¾“š°ø”æŅŅ>¼×>±ū ½µĪĀ½į¾§ ²»±„ŗĶ ¼× ²»Č·¶Ø
”¾½āĪö”æ
(1)øł¾ŻČܽā¶ČĒśĻßæÉÖŖ£¬30”ꏱ£¬¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹµÄČܽā¶ČÓɓ󵽊”µÄĖ³ŠņŹĒŅŅ>¼×>±ū£»
(2) øł¾ŻČܽā¶ČĒśĻßæÉÖŖ£¬¼×µÄČܽā¶ČŹÜĪĀ¶ČÓ°Ļģ½Ļ“󣬵±¼×ÖŠ»ģÓŠÉŁĮæµÄŅŅŹ±£¬æɲÉÓĆ½µĪĀ½į¾§·½·ØĢį“æ¼×£»
(3)30”ꏱ£¬¼×µÄČܽā¶Č½Ó½ü30g£¬Čō½«10g¼×ĪļÖŹ¼ÓČėµ½Ź¢ÓŠ50gĖ®µÄÉÕ±ÖŠ£¬³ä·ÖČܽāŗó£¬ĖłµĆČÜŅŗŹĒ²»±„ŗĶČÜŅŗ£»
(4)50”ꏱ£¬¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹµÄČܽā¶ČÓɓ󵽊”µÄĖ³ŠņŹĒ¼×>ŅŅ>±ū£»±„ŗĶČÜŅŗČÜÖŹÖŹĮæ·ÖŹżÓɓ󵽊”ŅĄ“ĪŹĒ¼×”¢ŅŅ”¢±ū£¬ÅäÖĘČżÖÖĪļÖŹµÄ±„ŗĶČÜŅŗĻąµČÖŹĮæ¾łĪŖ100g£¬ĖłŠčĖ®µÄÖŹĮæ×īÉŁµÄŹĒ¼×£»
(5)øł¾ŻČܽā¶ČĒśĻߣ¬±ūµÄČܽā¶ČĖęĪĀ¶ČÉżø߶ų¼õŠ”£¬ČōĻėÅŠ¶ĻÉżĪĀ¹ż³ĢŹĒ·ńÓŠ¹ĢĢåĪö³ö£¬ŠčŅŖÖŖµĄČÜŅŗŹĒ·ń±„ŗĶ£¬¶ųĢāøÉƻӊÖøĆ÷£¬¹ŹĢī£ŗ²»Č·¶Ø”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøÖĢśŹĒÖŲŅŖµÄ½šŹō²ÄĮĻ£¬ŌŚÉś²ś”¢Éś»īÖŠÓŠ¹ć·ŗµÄÓĆĶ¾”£½ØŌģ±±¾©°ĀŌĖ»įÖ÷ĢåÓż³””°Äń³²”±£¬¾ĶŹĒÓĆĮĖ“óĮæµÄøÖĢś”£
£Ø1£©ĆæÄźŹĄ½ēÉĻøÖĢśµÄ²śĮæŗÜøߣ¬øÖĢśµÄŠāŹ“Ņ²øųČĖĄą“ųĄ“ĮĖ¾Ž“óµÄĖšŹ§”£ĢśŌŚæÕĘųÖŠŠāŹ“£¬Źµ¼ŹÉĻŹĒĢśøśæÕĘųÖŠµÄ_____ŗĶ_____¹²Ķ¬×÷ÓĆµÄ½į¹ū£»
£Ø2£©ĪŖĮĖ·ĄÖ¹øÖĢśŠāŹ“£¬ČĖĆĒ³£²ÉÓĆŌŚĘä±ķĆęĶæĖ¢æóĪļÓĶ»ņ¶ĘÉĻĘäĖū½šŹōµČø²øĒ±£»¤Ä¤µÄ·½·Ø”£ÕāŠ©·½·Ø¶¼ÄÜ·ĄÖ¹ŠāŹ“µÄ¹²Ķ¬ŌĄķŹĒ_____£»
£Ø3£©Į¶Ģś³§³£ŅŌ½¹Ģ攢³ąĢśæó£ØÖ÷ŅŖ³É·ÖŹĒŃõ»ÆĢś£©æÕĘųµČĪŖÖ÷ŅŖŌĮĻĮ¶Ģś£¬·“Ó¦¹ż³ĢČēĻĀ£ŗĒėŠ“³öµŚ¢Ś²½·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_____”£
![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2ŌĀ20ČÕŌŚ¾©¾ŁŠŠµÄ¹śĪńŌŗĮŖ·ĄĮŖæŲ»śÖĘŠĀĪÅ·¢²¼»įÉĻ£¬ÖŠ¹ś¼²æŲÖŠŠÄŃŠ¾æŌ±·ėĀ¼ÕŁ±ķŹ¾£¬ŠĀ¹Ś·ĪŃ×COVID-19²”¶¾ĶعżĪŪČ¾ŅĀĪļøŠČ¾ČĖµÄ»śĀŹ¼«µĶ”£Čē¹ū²»ŹĒČ„¹żŅ½ŌŗµČĢŲ¶Ø³”Ėł£¬Ģ½ŹÓ¹ż²”ČĖ»ņÕß½Ó“„¹żæÉŅÉ֢דČĖŌ±£¬ĘÕĶع«ÖŚ²»ŠčŅŖ¶ŌŅĀ·ž×ØĆÅ¾Ę¾«Ļū¶¾”£·ėĀ¼ÕŁ½éÉÜ£¬¾Ę¾«¶ŌĘÕĶØŅĀĪļƻӊøÆŹ“×÷ÓĆ£¬µ«¾Ę¾«ŹĒ¼×ĄąŅ×Č¼ĪļĘ·£¬Čē¹ūÅēČ÷ŌŚŅĀĪļÉĻ£¬Óöµ½øßĪĀ”¢Ć÷»š”¢¾²µē¶¼æÉÄÜĘš»š£¬ĖłŅŌ½ØŅé²»ŅŖ½«¾Ę¾«ÅēČ÷ŌŚŅĀ·žÉĻ”£

£Ø1£©¾Ę¾«µÄѧĆū½ŠŅŅ“¼£¬ŹĒŅ»ÖÖÓŠ»śĪļ£¬»ÆѧŹ½ĪŖ_____£¬ŌŚ³£ĪĀ”¢³£Ń¹ĻĀŹĒĪŽÉ«ĶøĆ÷ŅŗĢ壬ӊ“Ģ¼¤ŠŌµÄ“¼ĻćĪ¶£¬ŹĒ¾ĘĄąŅūĘ·µÄÖ÷ŅŖ³É·Ö”£
£Ø2£©ŅŅ“¼ŅŗĢåĆܶȏĒ0.789g/cm3£Ø20”ę£©£¬ÄÜÓėĖ®ŅŌČĪŅā±Č»„ČÜ£¬Ņ²ŹĒĮ¼ŗƵÄÓŠ»śČܼĮ”£ŌŚ×ŌÖĘĖį¼īÖøŹ¾¼Į¹ż³ĢÖŠŠčŅŖĢķ¼Ó¾Ę¾«ČÜŅŗ£¬Ģķ¼Ó¾Ę¾«ČÜŅŗµÄ×÷ÓĆŹĒ_____”£
£Ø3£©75%£ØĢå»ż·ÖŹż£©µÄ¾Ę¾«³£ÓĆÓŚŅ½ĮĘĻū¶¾£¬ŅņĘäŌŚÓöµ½øßĪĀ”¢Ć÷»š”¢¾²µēŹ±¶¼æÉÄÜĘš»š£¬ĖłŅŌŹ¹ÓĆŹ±ŅŖĢŲ±šŠ”ŠÄ£»ČōÕżŌŚÅē³öµÄ¾Ę¾«ÓöĆ÷»šČ¼ÉÕøü¾ēĮŅ£¬ÉõÖĮ²śÉś±¬Č¼£¬²śÉś±¬Č¼µÄŌŅņŹĒ_____”£
£Ø4£©¾Ę¾«ŹĒŅŌÅ©×÷ĪļµÄ½ÕøŃ»ņĮøŹ³ĪŖŌĮĻ£¬ĶعżĪ¢ÉśĪļµÄ·¢½Ķ¶ųÖĘµĆ£¬Ņņ“Ė¾Ę¾«ŹōÓŚ_____£ØĢī”°æÉŌŁÉś”±»ņ”°²»æÉŌŁÉś”±£©ÄÜŌ“”£·¢½ĶµĆµ½µÄ¾Ę¾«æÉŅŌÓĆĄ“ÄšÖĘ°×¾Ę£¬µ«¹¤Ņµ¾Ę¾«Ņņŗ¬ÉŁĮæµÄ¼×“¼£ØCH3OH£©¶ų²»ÄÜÖĘ¾Ę”£¼×“¼ÓŠ¶¾£¬ĘäĖüµÄŠŌÖŹÓėŅŅ“¼Ź®·ÖĻąĖĘ£¬ŗÜÄŃ³żČ„£¬¹¤Ņµ¾Ę¾«ĶłĶłÓĆĄ“×öČ¼ĮĻ£¬Š“³ö¼×“¼Č¼ÉյĻÆѧ·½³ĢŹ½_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij°ąĶ¬Ń§ŌŚŹµŃéŹŅÖĘČ”¶žŃõ»ÆĢ¼£¬ĄĻŹ¦¹Ū²ģµ½ĮĖĖÄøöĶ¬Ń§µÄČēĻĀ²Ł×÷£¬ĘäÖŠÕżČ·µÄŹĒ£Ø £©
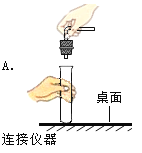
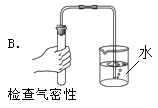
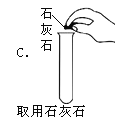
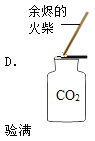
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×ŅŅĮ½ÖÖ²»ŗ¬½į¾§Ė®µÄ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻßČēĻĀĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
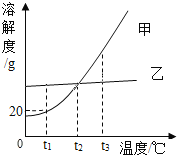
A.¼×µÄČܽā¶Č±ČŅŅ“ó
B.t1”ꏱ£¬100g¼×µÄ±„ŗĶČÜŅŗÖŠµÄČÜÖŹµÄÖŹĮæŹĒ20g
C.t2”ꏱ£¬¼×ŅŅµÄĮ½ÖÖ±„ŗĶČÜŅŗÖŠµÄČÜÖŹµÄÖŹĮæ·ÖŹżĻąµČ
D.½«µČÖŹĮæ¼×ŅŅµÄĮ½ÖÖČÜŅŗ·Ö±šÓÉt3”ę½µĪĀÖĮt2”ę£¬Īö³öµÄ¼×µÄÖŹĮæŅ»¶Ø±ČĪö³öµÄŅŅµÄÖŹĮæ“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓŠŅ»Ęæ±źĒ©ŹÜĖšµÄĪŽÉ«ČÜŅŗ£Ø±źĒ©ČēĶ¼ĖłŹ¾£©”£Ķ¬Ń§ĆĒ¾ö¶Ø¶ŌĘä³É·Ö½ųŠŠĢ½¾æ”£ĖūĆĒŹ×ĻČĻņĄĻŹ¦Ēė½Ģ£¬ĄĻŹ¦øęĖßĖūĆĒ³õÖŠ»ÆѧŹµŃéŹŅÖŠµÄŗ¬ÄĘ»ÆŗĻĪļæÉÄÜŹĒNaOH”¢NaCl”¢Na2SO4”¢NaNO3”¢Na2CO3”¢NaHCO£¬²¢øų³öĻą¹Ų׏ĮĻ£¬ČĆĶ¬Ń§ĆĒ½įŗĻĖłŃ§ÖŖŹ¶½ųŠŠĢ½¾æ”£
![]()
£ØĻą¹Ų׏ĮĻ£©(1)NaOH”¢Na2CO3”¢NaHCO3µÄČÜŅŗ³Ź¼īŠŌ£¬NaCl”¢Na2SO4”¢NaNO3µÄČÜŅŗ³ŹÖŠŠŌ”£
(2)NaHCO3ŹōÓŚæÉČÜĪļÖŹ£ØŹŅĪĀĻĀČܽā¶ČŠ”ÓŚ10g£©£¬¶ųĘäĖüĪļÖŹŹōÓŚŅ×ČÜĪļÖŹ£ØŹŅĪĀĻĀČܽā¶Č“óÓŚ10g£©”£
£Ø½»Į÷ĢÖĀŪ£©Ķ¬Ń§ĆĒŅ»ÖĀČĻĪŖøĆČÜŅŗŅ»¶Ø²»ŹĒNaHCO3ČÜŅŗ£¬ĖūĆĒµÄĄķÓÉŹĒ____”£
£ØŹµŃéĢ½¾æ£©ĪŖČ·¶ØøĆČÜŅŗµÄ³É·Ö£¬Ķ¬Ń§ĆĒ½ųŠŠĮĖČēĻĀŹµŃ锣
²½Öč | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
¢ń | ÓĆ²£Į§°ōÕŗČ”ČÜŅŗµĪµ½pHŹŌÖ½ÉĻ£¬°ŃŹŌÖ½ĻŌŹ¾µÄŃÕÉ«Óė____½ųŠŠ±Č½Ļ | ŹŌÖ½Ģõ±äĄ¶ | øĆČÜŅŗµÄpH=10£¬Ķعż±Č½Ļ”£æÉÄÜŹĒ____”£ |
¢ņ | ȔɣĮæČÜŅŗÓŚŹŌ¹ÜÖŠĻņĘäÖŠµĪ¼Ó×ćĮæµÄĻ”ŃĪĖį”£ | ____ | øĆČÜŅŗĪŖNa2CO3ČÜŅŗ”£ÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____”£ |
£Ø·“Ė¼ĘĄ¼Ū£©ĄĻŹ¦Öø³öøĆ½įĀŪ²»ŃĻĆÜ”£ĄķÓÉŹĒČōøĆČÜŅŗĪŖNaOHČÜŅŗ£¬ŌŚæÕĘųÖŠ·¢Éś±äÖŹ£¬Ņ²ÄܲśÉśÉĻŹöĻÖĻó”£ĒėŠ“³öNaOHŌŚæÕĘųÖŠ±äÖŹ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ®¼ŁĘŚ¼ä£¬Ä³ŠĖȤŠ”×éĶ¬Ń§¶Ō”°ŠæÓėĮņĖį·“Ó¦æģĀżµÄÓ°ĻģŅņĖŲ”±½ųŠŠĢ½¾æ”£
[Ģį³öĪŹĢā] ŠæÓėĮņĖį·“Ó¦µÄæģĀżÓėÄÄŠ©ŅņĖŲÓŠ¹Ų£æ
[²ĀĻė¼ŁÉč]£Ø1£©a”¢æÉÄÜÓėŠæµÄŠĪד”¢æÅĮ£“óŠ”ÓŠ¹Ų£»
b”¢æÉÄÜÓėĮņĖįµÄÖŹĮæ·ÖŹż“óŠ”ÓŠ¹Ų£»
c”¢»¹æÉÄÜÓė______ÓŠ¹Ų”£
[Éč¼ĘÓėŹµŃé] ŅŌ3·ÖÖÓÄŚŹÕ¼Æµ½µÄĒāĘųĢå»ż×÷ĪŖÅŠ¶ĻŅĄ¾Ż£¬¾ßĢåČēĻĀ±ķĖłŹ¾£ŗ
ŹµŃé ±ąŗÅ | ŠæµÄŠĪד £Ø¾łČ”1 g£© | ĮņĖįµÄÅØ¶Č £Ø¾łČ”20 mL£© | ĒāĘųµÄĢå»ż £Ø/mL£© |
¢Ł | ŠæĮ£ | 20% | 31.7 |
¢Ś | Šæʬ | 20% | 50.9 |
¢Ū | ŠæĮ£ | 30% | 61.7 |
¢Ü | Šæʬ | 30% |
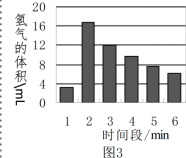
[±Č½Ļ·ÖĪö]£Ø2£©ŅŖŃéÖ¤²ĀĻėa £¬æÉŃ”ŌńµÄŹµŃ鱹ŗÅŹĒ_______________”£
£Ø3£©ŹµŃé¢ÜÓÉӌƻӊ¼°Ź±¼ĒĻĀŹż¾Ż£¬¾Ķ¬Ń§»ŲŅ䣬ÄćČĻĪŖ±Č½ĻæÉÄܵďżÖµŹĒ__________£ØĢī”°57.5”±»ņ”°75.5”±£©”£
[µĆ³ö½įĀŪ]£Ø4£©Ķź³ÉŹµŃé¢Ł¢Ś¢Ūŗó£¬æÉŅŌµĆ³öÓ°ĻģøĆ·“Ó¦æģĀżµÄŅ»Ģõ½įĀŪŹĒ£ŗ________”£
[·“Ė¼ĘĄ¼Ū] Ķ¼3ŹĒÓĆŹµŃé¢ŁĄ“²ā¶Ø£¬ŌŚĆæŅ»·ÖÖÓÄŚŹÕµ½ĒāĘųµÄĢå»ż±ä»ÆĶ¼£¬Ēė
£Ø5£©µŚ1·ÖÖÓŹ±¼äÄŚ·“Ó¦µÄĖŁĀŹ½ĻĀż£¬ÕāŹĒÓÉÓŚŠæĮ£±ķĆęÓŠŠ©Ńõ»ÆĤ£ØZnO£©ø²øĒ£¬ŌņĘäŌŅņÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ______”£
£Ø6£©“ÓµŚ3·ÖÖÓæŖŹ¼£¬·“Ó¦µÄĖŁĀŹÓÖÖš½„±ä______£¬ÕāŹĒŅņĪŖ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶Ō±ČѧĻ°ÓŠĄūÓŚ·¢ĻÖŹĀĪļµÄ¹²ŠŌÓėøöŠŌ”£ĪŖĢ½¾æĖįµÄŠŌÖŹ£¬Ķ¬Ń§ĆĒ½ųŠŠĮĖČēĻĀŹµŃ锣
ŹµŃéÄŚČŻ | ŹµŃéĻÖĻó | ·ÖĪöÓė½įĀŪ |
| “×Ėį¾§ĢåŹŌ¹ÜÄŚ___£¬“×ĖįČÜŅŗŹŌ¹ÜÖŠĆ¾“ų±ķĆęĆ°ĘųÅŻ”£ | ĖįµÄŗܶą·“Ó¦Ķس£ŌŚĖ®ČÜŅŗÖŠ²ÅÄÜĶź³É”£ |
ÓĆ²£Į§°ōÕŗĮņĖįŌŚ°×Ö½ÉĻŠ“×Ö | _______£ØĢī”°ÅØ”±»ņ”°Ļ””±£©ĮņĖįŹ¹°×Ö½Ģæ»Æ”£ | ¼“Ź¹ŹĒĶ¬ÖÖĖį£¬ÓÉÓŚ____²»Ķ¬£¬ĖüĆĒµÄŠŌÖŹ²»ĶźČ«ĻąĶ¬”£ |
| Į½ŹŌ¹ÜÖŠ¾ł²śÉś_____ | ²»Ķ¬µÄĖį¾ßÓŠĻąĖʵĊŌÖŹ£¬ÕāŹĒŅņĪŖĖįµÄ×é³ÉÖŠ¶¼ŗ¬ÓŠ_____£ØĢīŌŖĖŲ·ūŗÅ£©”£ |
| EŹŌ¹ÜÖŠ²śÉś_____£¬ FŹŌ¹ÜÖŠĪŽĆ÷ĻŌĻÖĻó”£ | ²»Ķ¬µÄĖįøł»įµ¼ÖĀĖįµÄ”°øöŠŌ”±²īŅģ”£Ņņ“Ė£¬æÉÓĆĀČ»Æ±µČÜŅŗ¼ų±šŃĪĖįŗĶĮņĖį”£ |
ĒåĻ“ŹŌ¹ÜŹ±£¬Š”ĒĒĶ¬Ń§½«C”¢FĮ½ŹŌ¹ÜÖŠµÄĪŽÉ«ŅŗĢåĶ¬Ź±µ¹ČėŅ»øö½ą¾»µÄ·ĻŅŗø×£¬·ĻŅŗø×ÖŠĮ¢æĢĆ°ĘųÅŻ²¢³öĻÖ°×É«³Įµķ”£Ēė·ÖĪöÉĻŹöĻÖĻó²¢»Ų“š£ŗ
¢ń.·ĻŅŗø×ÖŠ²śÉśĘųĢåµÄ»Æѧ·½³ĢŹ½ĪŖ______”£
¢ņ. ·ĻŅŗøץļ×īÖÕ²śÉśµÄ°×É«³ĮµķÖŠŅ»¶ØÓŠĮņĖį±µ£¬æÉÄÜÓŠ____£ØĢī»ÆѧŹ½£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒČżÖÖĪļÖŹµÄČܽā¶ČĒśĻß”£Ēė»Ų“š:
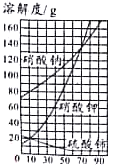
(1)Čܽā¶ČĖęĪĀ¶ČÉżø߶ų½µµĶµÄŹĒ_______£»30”ꏱČܽā¶Č×ī“óµÄŹĒ_______”£
(2)80”ꏱĻõĖįÄʱ„ŗĶČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ_______”£²»±„ŗĶČÜŅŗ±äĪŖ±„ŗĶČÜŅŗ£¬æɲÉČ”µÄ“ėŹ©ÓŠ_______(Š“Ņ»ÖÖ)”£
(3)ijĻõĖį¼Ų¹ĢĢåÖŠ»ģÓŠÉŁĮæĮņĖįīęŌÓÖŹ£¬·ÖĄėĢį“æĻõĖį¼ŲµÄ²Ł×÷ŹĒ:Åä³ÉøßĪĀĻĀµÄĻõĖį¼Ų±„ŗĶČÜŅŗ”¢_______”¢¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com